Trong các loại bệnh ung thư, ung thư phổi gây tử vong hàng đầu hiện nay và là một trong những chỉ định điều trị chính sử dụng xạ trị proton. Chùm tia proton có sự phân bố liều vượt trội hơn các kỹ thuật khác và có tác động đến các mô rất nhạy với sự thay đổi về mặt giải phẫu. Cũng chính bởi đặc điểm đó, xạ trị proton có yêu cầu cao đối với việc lập kế hoạch điều trị để đảm bảo khu vực chiếu xạ được tối ưu và giảm tác hại đến mô lành trên cơ thể bệnh nhân.
Ung thư phổi tiếp tục là nguyên nhân gây tử vong hàng đầu trong các loại bệnh ung thư hiện nay, chỉ riêng ở Hoa Kỳ, trong năm 2015 đã có hơn 158.000 ca tử vong. Xạ trị là một trong những phương thức điều trị chính trong điều trị ung thư phổi. Do phạm vi giới hạn của chùm tia proton, xạ trị proton (sử dụng chum tia proton – PBT) ngày càng được sử dụng nhiều cho bệnh ung thư phổi. So với kỹ thuật xạ trị điều biến liều sử dụng bức xạ photon (IMRT), xạ trị proton có thể giảm tác động xấu tới phổi, thực quản, tim, thần kinh và các mô lành khác tốt hơn với cùng một liều chiếu hoặc thậm chí với liều cao hơn tới khối U. Lợi thế về liều lượng của xạ trị proton mang đến khả năng kiểm soát khối u tốt hơn và ít độc tính hơn.
Hệ thống xạ trị proton
Tùy thuộc vào cách chùm tia proton được phát tán theo chiều ngang và chiều sâu, chủ yếu hiện có 03 hệ thống xạ trị proton trong ứng dụng lâm sàng: xạ trị proton tán xạ thụ động (PSPT), xạ trị proton quét chùm tia đồng đều (USPT) và xạ trị proton quét chùm tia dạng bút chì (PBS). Trong PSPT, chùm proton được trải ra theo phương ngang bởi một bộ tán xạ tĩnh (hoặc bộ tán xạ kép) nằm trong trục chuẩn trực và điều phối theo chiều sâu bằng cách kiểm soát dải quay với nhiều bước khác nhau. Cả xạ trị proton USPT và PBS đều sử dụng nam châm quét để quét các chùm tia proton theo chiều ngang và phân bố liều lượng tới từng lớp thể tích của mục tiêu ở các độ sâu khác nhau bằng cách sử dụng các chùm tia proton có năng lượng khác nhau. Sự khác biệt chính giữa USPT và PBS là các chùm tia proton được quét liên tục với cường độ đồng đều theo mô hình ziczac ở một tần số cố định cho mỗi lớp năng lượng trong USPT và phân phối với các cường độ khác nhau từ điểm này sang điểm khác hoặc liên tục cho mỗi lớp trong PBS. PBS có thể phân phối liều đồng nhất dạng trường đơn (SFUD – cung cấp liều lượng đồng nhất) và phân phối liều đồng nhất đa trường (MFUD – cung cấp liều không đồng nhất nhưng đạt được liều kết hợp đồng nhất từ tất cả các lớp). MFUD còn được gọi là xạ trị proton điều biến liều (IMPT).
Đối với xạ trị USPT: Chùm tia proton đi qua một chất làm suy giảm năng lượng và một hệ thống chọn lọc năng lượng (ESS), sau đó được đưa đến một ống truyền tia trong phòng điều trị. Sau khi đi vào ống truyền tia, chùm proton sẽ đi qua bộ tán xạ thứ nhất, mở rộng phạm vi để đạt được kích thước khu vực tác động mong muốn. Sau đó, chùm tia đi qua một bộ điều biến phạm vi, bộ phận này này không quay liên tục mà chủ yếu đóng vai trò làm suy giảm năng lượng. Cùng với bộ tán xạ đầu tiên, bộ điều chế làm giảm năng lượng proton cung cấp liều lượng theo từng lớp chiều sâu. Chùm tia được quét theo phương ngang với tần số không đổi bởi hai nam châm quét theo hình ziczac để có một liều đồng đều cho vùng quét dạng hình chữ nhật. Sau đó, chum tia proton đi qua buồng ion hóa chính và dự phòng để theo dõi liều lượng proton. Ở cuối ống truyền tia là một thiết bị giữ khẩu độ và bù, có thể di chuyển dọc theo trục chùm tia ở các vị trí đẳng tâm. Một bộ chuẩn trực chùm tia theo chiều ngang và một bộ bù phạm vi được sử dụng để điều chỉnh mức độ tác động của proton đến mục tiêu điều trị.
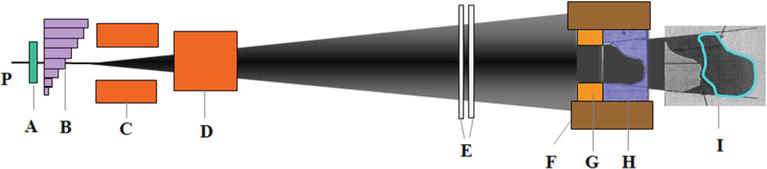
Sơ đồ của ống quét đồng nhất: Chùm proton (P) đi qua bộ tán xạ thứ nhất (A), bộ điều biến phạm vi (B), hai nam châm quét (C và D), buồng ion hóa chính và dự phòng (E), thiết bị giữ khẩu độ (F), bộ khẩu độ (G), bộ bù phạm vi (H) và điểm dừng ở bệnh nhân (I).
Phương pháp tiến hành
Việc đảm bảo giữ yên bệnh nhân và lập mô phỏng khi điều trị bằng proton cũng tương tự như khi điều trị các kỹ thuật xạ trị sử dụng photon. Tuy nhiên, vì chùm proton rất nhạy với sự chuyển động của bệnh nhân, nên khả năng giữ cố định và quản lý chuyển động của bệnh nhân là rất quan trọng trong xạ trị proton. Bệnh nhân thường được đặt nằm ngửa, giữ bất động bằng túi hút chân không trên thiết bị có khung cố định, hai tay giơ lên bám vào các chốt trên giường nằm điều trị. Bệnh nhân được quét với độ dày lát cắt là 2,5 mm.
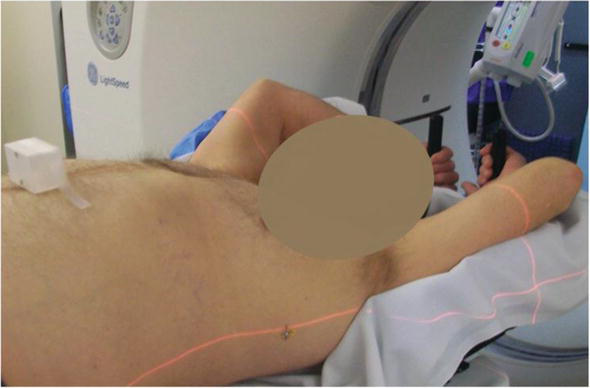
Kỹ thuật mô phỏng và cố định điển hình trong điều trị ung thư phổi sử dụng xạ trị proton quét đồng nhất.
Chụp cắt lớp vi tính (CT) bốn chiều (4D) thường được sử dụng cho bệnh nhân ung thư phổi trong xạ trị proton để đánh giá chuyển động của bệnh nhân. Chuyển động có thể được theo dõi bằng hệ thống dây đai hoặc hệ thống Varian RPM trong quá trình chụp CT 4D. Mức độ chuyển động thường được đánh giá cho mỗi lần chụp CT 4D và được sử dụng để xác định kế hoạch trong quản lý chuyển động. Tùy thuộc vào cơ sở và hệ thống phân phối chùm tia, giới hạn về cường độ chuyển động sẽ được thiết lập và sau đó bệnh nhân sẽ được quản lý chuyển động bổ sung hoặc không được xạ trị proton nếu vượt quá giới hạn cho phép.
Hướng đi trong tương lai
Công nghệ xạ trị proton đang phát triển rất nhanh chóng và có nhiều tiến bộ nhằm hướng tới việc điều trị chính xác và hiệu quả hơn. PBS ngày càng được sử dụng nhiều trong điều trị ung thư phổi. Sự tiến bộ của cả PBS và CT đã cho phép việc lập kế hoạch xạ trị trực tuyến có thể thực hiện được trong xạ trị proton. Việc lập kế hoạch điều trị là cần thiết cho xạ trị proton đối với bệnh ung thư phổi, nhưng tiêu tốn nhiều thời gian và không phải bệnh nhân nào cũng có thể đáp ứng được điều này. Do đó, việc dự đoán khi nào cần lập kế hoạch và cho những bệnh nhân nào là rất cần thiết. Điều này sẽ cho phép quy trình lập kế hoạch được cá nhân hóa cho bệnh nhân, nâng cao hiệu quả điều trị, tiết kiệm chi phí, giảm rủi ro sai sót điều trị từ quá trình điều chỉnh kế hoạch và loại bỏ liều lượng không cần thiết cho bệnh nhân khi chụp CT.
Từ khóa: Xạ trị proton; lập kế hoạch xạ trị; ung thư phổi;
– CMD&DND –