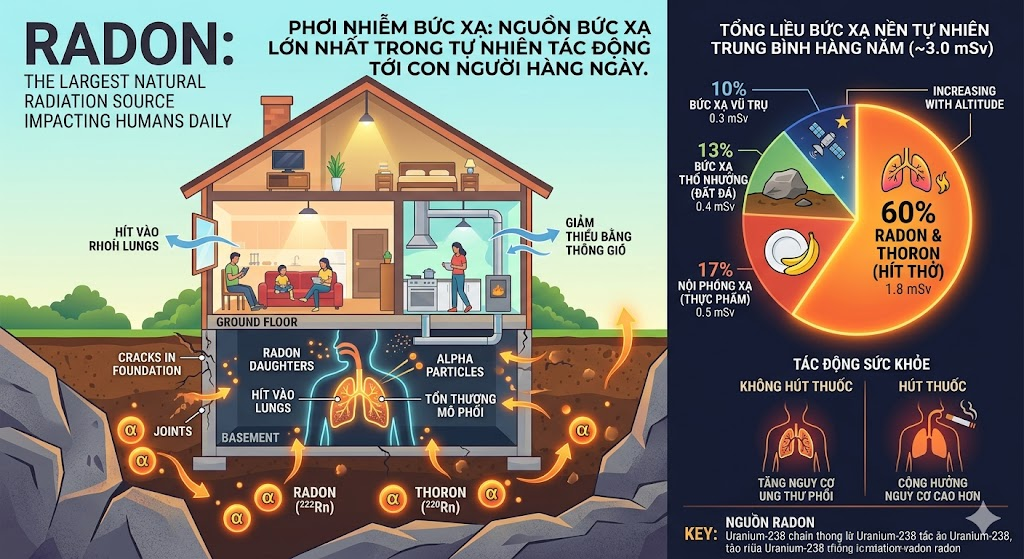
Liệu pháp bức xạ (Xạ trị – RT) giữ vai trò không thể thay thế trong quản lý đa phương thức ung thư vú, được áp dụng sau phẫu thuật bảo tồn vú (BCS) hoặc sau đoạn nhũ (mastectomy) để giảm nguy cơ tái phát. Trong hơn hai thập kỷ qua, lĩnh vực xạ trị đã trải qua một sự chuyển đổi đáng kể, từ các phác đồ phân liều kéo dài đến các phác đồ rút gọn, chính xác và được cá nhân hóa cao. Vai trò nền tảng của xạ trị cũng được củng cố qua các phân tích tổng hợp quy mô lớn, các báo cáo từ Nhóm Hợp tác Thử nghiệm Ung thư Vú giai đoạn sớm (EBCTCG) đã cung cấp dữ liệu định lượng chính xác về lợi ích của xạ trị sau BCS.
Các nghiên cứu này chỉ ra rằng, sau phẫu thuật bảo tồn, xạ trị bổ trợ vào vú giảm một nửa (50%) tỷ lệ bệnh tái phát và giảm khoảng một phần sáu (1/6) tỷ lệ tử vong do ung thư vú sau 15 năm theo dõi. Tuy nhiên, điều quan trọng là lợi ích (absolute benefit) từ xạ trị có sự khác biệt đáng kể tùy thuộc vào đặc điểm sinh học và lâm sàng của bệnh nhân. Hiểu rõ sự khác biệt trong lợi ích tuyệt đối này là yếu tố cốt lõi để cá nhân hóa việc ra quyết định điều trị, đặc biệt trong việc xác định các nhóm bệnh nhân có nguy cơ thấp có thể cân nhắc bỏ qua xạ trị (de-escalation).
Sự thay đổi lớn nhất trong thực hành xạ trị ung thư vú trong hai thập kỷ qua là việc áp dụng xạ trị phân liều rút gọn (Hypofractionated Radiation Therapy – HRT) như là tiêu chuẩn trong điều trị. Sự thay đổi này được dựa trên sự hiểu biết sâu sắc hơn về cơ sở sinh học bức xạ của ung thư vú. Theo mô hình Quadratic tuyến tính (Linear-Quadratic Model – LQ), phản ứng của mô đối với sự thay đổi kích thước phân liều được mô tả bằng tỷ số alpha\beta. Các mô khối u và mô lành có phản ứng muộn thường có tỷ số alpha\beta thấp (khoảng 3-5 Gy). Các thử nghiệm lâm sàng lớn tại Anh, gọi là thử nghiệm START A và START B, đã cung cấp bằng chứng thuyết phục cho sự chuyển đổi này.
Thử nghiệm START đã so sánh phác đồ xạ trị tiêu chuẩn lịch sử (50 Gy trong 25 phân liều, 2 Gy/F) với các phác đồ phân liều rút gọn (ví dụ: 40 Gy trong 15 phân liều, 2.67 Gy/F). Kết quả chỉ ra rằng phác đồ phân liều rút gọn mang lại kết quả kiểm soát u tại chỗ/tại vùng và độc tính mô lành muộn tương đương hoặc tốt hơn. Dữ liệu từ START A và B ước tính giá trị alpha\beta điều chỉnh cho kiểm soát khối u là 4.6 Gy và cho thay đổi muộn về ngoại hình vú (late change in breast appearance) là 3.4 Gy. Việc giá trị alpha\beta của khối u ung thư vú (đặc biệt là các loại phản ứng tốt với nội tiết) được xác định là thấp, gần với mô lành phản ứng muộn, là cơ sở khoa học then chốt cho việc áp dụng phân liều rút gọn. Nếu alpha\beta của khối u cao hơn đáng kể, liều phân liều lớn hơn sẽ làm giảm hiệu quả kiểm soát u. Tuy nhiên, bằng chứng lâm sàng chứng minh hiệu quả tương đương giữa phân liều lớn và phân liều nhỏ đã buộc giới chuyên môn phải thừa nhận rằng ung thư vú đáp ứng với sự thay đổi phân liều tương tự như mô lành muộn. Điều này đã hợp lý hóa việc chuyển sang HRT, cho phép hoàn thành quá trình điều trị trong thời gian ngắn hơn (3 tuần so với 5-6 tuần) mà không làm tăng nguy cơ độc tính muộn.
Chỉ định xạ trị bổ trợ phải được quyết định trong môi trường đa chuyên khoa, dựa trên giai đoạn bệnh, loại phẫu thuật, và các yếu tố nguy cơ của bệnh nhân, theo các hướng dẫn quốc tế như ASTRO, ASCO, và NCCN. Các hướng dẫn gần đây, đặc biệt là bản cập nhật 2025 về Xạ trị Sau Đoạn nhũ (PMRT), đã tinh chỉnh việc lựa chọn bệnh nhân trong kỷ nguyên điều trị tân bổ trợ. Xạ trị toàn bộ vú (Whole Breast Irradiation – WBI) sau BCS là tiêu chuẩn điều trị bắt buộc cho hầu hết bệnh nhân ung thư vú xâm lấn giai đoạn sớm và cho ung thư biểu mô ống tuyến tại chỗ (Ductal Carcinoma In Situ – DCIS) để giảm đáng kể nguy cơ tái phát tại chỗ. WBI làm giảm nguy cơ tái phát tại chỗ của DCIS từ 50-60%. Trong một số trường hợp được lựa chọn cẩn thận (thường là bệnh nhân cao tuổi 70, giai đoạn I, ER dương tính, nguy cơ thấp), có thể cân nhắc điều trị nội tiết đơn thuần mà không cần xạ trị bổ trợ. Tuy nhiên, quyết định này cần được cân nhắc kỹ lưỡng với bệnh nhân (shared decision making).
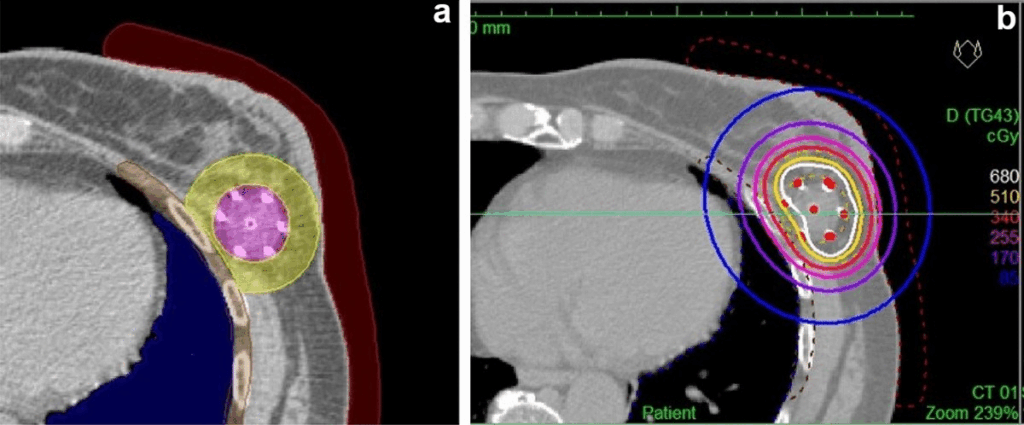
PMRT được chỉ định để giảm nguy cơ tái phát cục bộ và cải thiện tỷ lệ sống sót chung. Bằng chứng từ EBCTCG năm 2018 cho thấy sau đoạn nhũ và nạo vét hạch nách, xạ trị giảm tái phát và tử vong không chỉ ở phụ nữ có di căn nhiều hạch bạch huyết mà còn ở những người chỉ có 1-3 hạch nách dương tính. Các khuyến nghị cập nhật từ ASTRO/ASCO/SSO năm 2025 đã làm rõ các chỉ định, đặc biệt sau khi bệnh nhân trải qua hóa trị tân bổ trợ (Neoadjuvant Systemic Therapy – NACT). Việc quyết định PMRT cho bệnh nhân sau NACT đã trở nên cá nhân hóa hơn. Hướng dẫn 2025 nhấn mạnh rằng đối với bệnh nhân ban đầu có khối u nhỏ (cT1-2N0) nhưng đạt được đáp ứng bệnh học hoàn toàn ở vú và hạch (ypT0N0), PMRT thường không được khuyến nghị. Sự thay đổi này phản ánh sự công nhận rằng đối với nhóm bệnh nhân đáp ứng hoàn toàn, nguy cơ tái phát tại chỗ/tại vùng đã giảm xuống mức thấp, cho phép bỏ qua xạ trị bổ trợ để tránh các độc tính lâu dài, đặc biệt là độc tính trên tim mạch, trong khi vẫn duy trì hiệu quả kiểm soát bệnh.
Chỉ định xạ trị sau đoạn nhũ (PMRT) – Khuyến nghị quốc tế 2025
| Tình trạng Bệnh lý | Chỉ định PMRT | Phạm vi Chiếu Xạ | Mức độ Khuyến cáo |
| Hạch nách dương tính (pN+) | Khuyến nghị | Thành ngực/Vú tái tạo và hạch vùng | Mạnh (Strong) |
| Khối u lớn pT3-4, ngay cả khi pN0 | Khuyến nghị | Thành ngực/Vú tái tạo và hạch vùng | Mạnh (Strong) |
| Diện cắt dương tính sau đoạn nhũ | Khuyến nghị có điều kiện | Thành ngực/Vú tái tạo | Có điều kiện |
| Sau NACT, đáp ứng hoàn toàn (ypT0N0), ban đầu cT1-2N0 | Không khuyến nghị | Không cần PMRT | Mạnh (Strong) |
| Sau NACT, di căn hạch còn sót lại (ypN+) | Khuyến nghị | Thành ngực/Vú tái tạo và hạch vùng | Mạnh (Strong) |
Xạ trị cũng được áp dụng cho các trường hợp bệnh phức tạp hoặc tiến triển:
- Ung thư vú thể viêm (Inflammatory Breast Cancer): Đây là một loại ung thư nguy hiểm, thường được điều trị bằng hóa trị tân bổ trợ, tiếp theo là đoạn nhũ và sau đó là xạ trị bổ trợ bắt buộc toàn bộ thành ngực và hạch vùng để giảm nguy cơ tái phát rất cao.
- Ung thư vú di căn (Palliative Radiotherapy): Khi ung thư đã lan sang các bộ phận khác của cơ thể, xạ trị được sử dụng để giảm triệu chứng, thu nhỏ khối u, và giảm đau do di căn xương, nhằm cải thiện đáng kể chất lượng cuộc sống (QOL) của bệnh nhân. Xạ trị giảm nhẹ là một phần quan trọng của chăm sóc toàn diện trong điều trị ung thư di căn.
Xạ trị một phần vú tăng tốc (Accelerated Partial Breast Irradiation – APBI): là một chiến lược điều trị cho phép cung cấp bức xạ liều cao, tập trung, chỉ vào vùng giường khối u, nơi có nguy cơ tái phát cục bộ cao nhất, thay vì toàn bộ mô vú. Phương pháp này chỉ dành cho một nhóm nhỏ bệnh nhân ung thư vú giai đoạn sớm, nguy cơ tái phát thấp. Do APBI không chiếu xạ toàn bộ vú, việc lựa chọn bệnh nhân phải tuân thủ các tiêu chuẩn nghiêm ngặt để đảm bảo an toàn về mặt ung thư học. Hướng dẫn ASTRO 2023 đã xác định rõ ràng các tiêu chí này.
Tiêu chuẩn lựa chọn bệnh nhân tiềm năng cho APBI
| Tiêu chí | Yêu cầu Khuyến nghị (ASTRO/ASBS) |
| Loại Phẫu thuật | Sau phẫu thuật bảo tồn vú (Lumpectomy) |
| Tuổi Bệnh nhân | Trên 60 (ASTRO) hoặc trên 40 (tùy theo hướng dẫn) |
| Kích thước Khối u (pT) | Trên 2 cm (ASTRO) hoặc trên 3 cm (ASBS/ABS) |
| Tình trạng Hạch (pN) | Hạch nách âm tính (N0) |
| Đặc điểm U | Carcinoma xâm lấn hoặc DCIS (Carcinoma ống tuyến tại chỗ), đơn ổ |
| Sinh học U | ER dương tính, HER2 âm tính, Độ mô học 1-2 |
| Bờ Phẫu thuật (Margins) | Âm tính. Không có u trên mực in đối với K xâm lấn; trên 2 mm đối với DCIS |
| LVSI | Không có xâm lấn mạch máu/bạch huyết (LVSI âm tính) |
APBI có thể được thực hiện bằng Xạ trị gần (Brachytherapy) hoặc Xạ trị chùm tia ngoài (EBRT APBI).
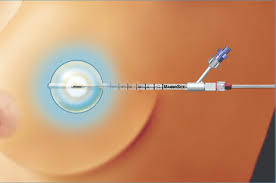
- Xạ trị gần (Brachytherapy APBI):
- Đây là kỹ thuật có bằng chứng lâm sàng mạnh mẽ nhất, sử dụng liệu pháp xạ trị gần liều cao (HDR), thường thông qua kỹ thuật kẽ nhiều ống thông hoặc các thiết bị áp dụng đơn kênh.
- Một thử nghiệm ngẫu nhiên đa trung tâm ở Châu Âu so sánh WBI và APBI (Brachytherapy) ở ung thư vú giai đoạn đầu cho thấy kết quả tương đương về tái phát tại chỗ, sống sót không bệnh tật (DFS) và sống sót toàn bộ (OS) sau 5 năm.
- Đáng chú ý, APBI bằng xạ trị gần cho thấy tỷ lệ kết quả thẩm mỹ Tốt/Xuất sắc cao hơn (81%) so với WBI (63%).
- Xạ trị chùm tia ngoài (EBRT APBI):
- Mặc dù tiện lợi hơn về mặt kỹ thuật lắp đặt so với xạ trị gần kẽ, một số thử nghiệm lâm sàng ngẫu nhiên đã báo cáo tỷ lệ kết quả thẩm mỹ kém hơn với EBRT APBI so với WBI.
- Sự khác biệt về kết quả thẩm mỹ này được cho là do sự dịch chuyển của bệnh nhân và hô hấp, buộc các nhà vật lý y tế phải mở rộng thể tích chiếu xạ (planning target volume – PTV) lớn hơn đáng kể so với kỹ thuật xạ trị gần. Xạ trị gần, với gradient liều dốc và liều bên ngoài vú cực thấp, bảo tồn mô vú lành tốt hơn đáng kể. Việc đảm bảo tính đồng nhất của liều bức xạ đến mô vú còn lại là yếu tố quyết định chất lượng thẩm mỹ lâu dài, và xạ trị gần có vẻ vượt trội hơn trong khía cạnh này.
Từ khóa: xạ trị;
– CMD –