Phương pháp điều trị ung thư nhằm mục đích tiêu diệt tế bào ung thư. Các phương pháp bổ trợ thường được sử dụng để giúp những người mắc bệnh ung thư, gọi là liệu pháp hỗ trợ, bảo vệ các mô lành hoặc giảm các tác dụng phụ của phương pháp điều trị ung thư. Điều gì sẽ xảy ra nếu một loại thuốc có thể đóng cả hai vai trò này cùng một lúc? Trong các nghiên cứu mới trên chuột, các nhà nghiên cứu phát hiện ra rằng một loại thuốc gọi là avasopasem mangan (AVA), được chứng minh là có tác dụng bảo vệ các mô bình thường khỏi bức xạ, cũng có thể làm cho các tế bào ung thư dễ bị tổn thương hơn khi điều trị bằng bức xạ.
Douglas Spitz, Tiến sĩ, giáo sư về xạ trị ung thư tại Đại học Iowa, đứng đầu nghiên cứu, giải thích: AVA mang lại tác dụng kép này bằng cách khai thác sự khác biệt trong cách tế bào bình thường và tế bào khối u sản xuất hydro peroxide. Với bất kỳ phương pháp điều trị ung thư nào, “cố gắng tìm ra điểm lợi thế này, nơi cân bằng giữa liều điều trị để tiêu diệt tế bào ung thư nhưng không gây tổn hại quá mức cho các mô bình thường,”. Nếu có thể có một loại thuốc làm giảm độc tính trong các mô bình thường đồng thời tăng độc tính trong tế bào ung thư, thì thực sự sẽ làm thay đổi các liệu pháp điều trị hiện nay. Cần nhiều nghiên cứu hơn để xem liệu những tác động quan sát được ở chuột có thể được nhân rộng ở người hay không. Tháng 4/2024, Galera Therapeutics, công ty sản xuất AVA, đã phát hiện những dấu hiệu tích cực của AVA từ một thử nghiệm lâm sàng được bổ sung vào xạ trị có mục tiêu ở những người bị ung thư tuyến tụy. Hai thử nghiệm lâm sàng khác cũng đang diễn ra về AVA kết hợp với xạ trị trong ung thư phổi và tuyến tụy.
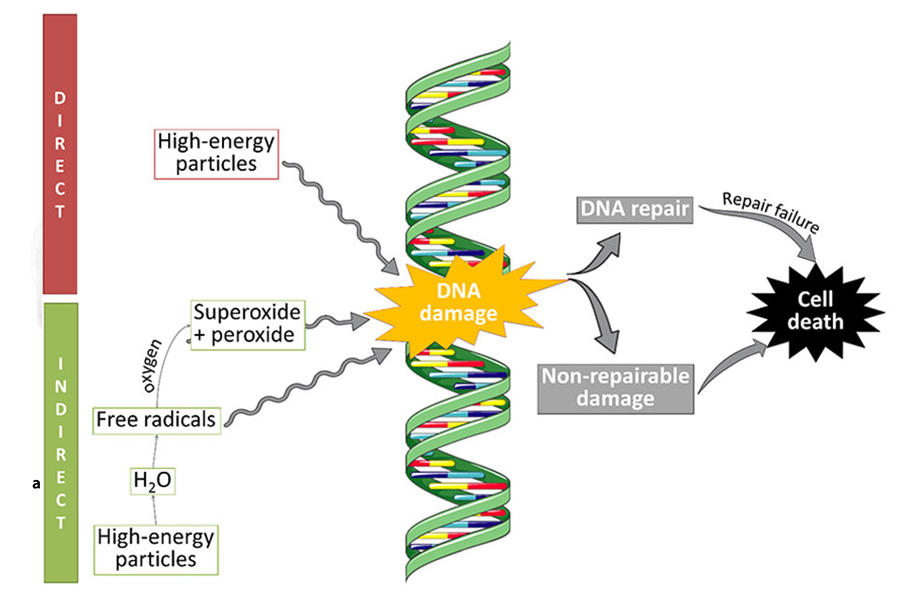
Xạ trị có thể làm tổn hại trực tiếp DNA hoặc gián tiếp làm tổn thương DNA thông qua việc tạo ra các gốc tự do (Nguồn: Chuyển thể từ Frontiers in Pharmacology. Tháng 8 năm 2019. https://doi.org/10.3389/fphar.2019.00851. CC-BY-4.0)
Trong xạ trị, người ta sử dụng tia bức xạ liều cao hoặc các hạt tích điện nhắm vào khối u. Bức xạ có thể làm hỏng DNA của tế bào ung thư đến mức tế bào ngừng phân chia hoặc chết. Trong khi một liều bức xạ được thực hiện chỉ vài phút, thì những thay đổi dẫn đến tế bào chết phải mất nhiều ngày mới xảy ra. Khi một liều bức xạ chiếu vào tế bào, năng lượng cao của nó sẽ tạo ra các hợp chất gọi là gốc tự do có thể làm hỏng nhiều bộ phận của tế bào, bao gồm cả DNA. Ví dụ: phân tử nước bao gồm hai nguyên tử hydro và một nguyên tử oxy: H2O. Một chùm bức xạ có thể tách các nguyên tử hydro ra khỏi các phân tử nước trong tế bào. Sự mất mát các nguyên tử hydro này gây ra hiệu ứng domino, bắt đầu bằng việc tạo ra các gốc tự do, từ đó thúc đẩy quá trình sản xuất hydro peroxide, có thể làm hỏng DNA. Các hợp chất trong tế bào được gọi là chất nhặt gốc tự do bảo vệ chúng khỏi mức độ sản sinh và tổn hại gốc tự do bình thường. AVA bắt chước một loại enzym nhặt gốc tự do tự nhiên được gọi là SOD. Những enzyme này chuyển đổi một gốc tự do gọi là superoxide thành hydro peroxide và oxy. Trong các tế bào bình thường, hydrogen peroxide được loại bỏ bởi các enzym khác. Nhưng trong các tế bào ung thư, do quá trình trao đổi chất bị tổn hại nên hydro peroxide không được loại bỏ, gây ra sự hình thành thêm các gốc tự do gây tổn hại DNA.
AVA bắt chước điều gì đó của cơ thể, nhưng đã được thiết kế để thực hiện điều đó hiệu quả hơn. Theo đó, loại thuốc này được gọi là thuốc bắt chước SOD. Trong một thử nghiệm lâm sàng gần đây, điều trị bằng AVA đã được chứng minh là làm giảm đáng kể tình trạng viêm niêm mạc, vết loét trong miệng do xạ trị và hóa trị ở những người đang điều trị ung thư đầu và cổ. Tuy nhiên, tác dụng của mô phỏng SOD đối với tế bào ung thư vẫn chưa được kiểm tra chặt chẽ. Tiến sĩ Spitz giải thích: “Người ta dự đoán rằng mô phỏng SOD sẽ bảo vệ mô bình thường và làm nhạy cảm mô khối u do sự khác biệt về sinh học gốc tự do giữa hai loại này. Đối với AVA, sự khác biệt chính quan trọng là các tế bào ung thư tiếp xúc với quá trình bức xạ superoxide và các gốc tự do khác kém hiệu quả hơn nhiều. Vì vậy, trong khi AVA bảo vệ các tế bào bình thường bằng cách loại bỏ superoxide mà chúng tạo ra để phản ứng với bức xạ, thì nó có thể có tác dụng ngược lại đối với các tế bào ung thư. Bằng cách biến superoxide của chúng thành các chùm hydro peroxide, việc điều trị bằng AVA có khả năng làm tăng tác động gây tổn hại DNA của bức xạ trong các tế bào ung thư.
Để thử nghiệm ý tưởng này, hai nhóm nghiên cứu đã nuôi cấy tế bào ung thư phổi không phải tế bào nhỏ ở người ở chân chuột, sau đó điều trị chúng bằng bức xạ, có hoặc không có AVA. Các khối u co lại nhiều hơn ở những con chuột nhận được AVA ngay trước khi xạ trị so với những con chuột chỉ nhận bức xạ. Khi bổ sung liều AVA cho chuột hàng ngày trong 4 ngày sau khi xạ trị – trong thời gian các tế bào ung thư có thể sản xuất superoxide – hiệu quả đã tăng lên rất nhiều, với nhiều khối u biến mất hoàn toàn. Điều thú vị là hiệu ứng này phụ thuộc vào độ lớn của liều bức xạ sử dụng. Nghĩa là, các thí nghiệm bổ sung cho thấy AVA chỉ tăng cường phản ứng với bức xạ khi bức xạ đó được cung cấp ở liều cao hơn, chẳng hạn như mức độ có thể được nhìn thấy bằng một dạng bức xạ được phân phối chính xác hơn gọi là liệu pháp bức xạ cơ thể lập thể (SBRT), tức là thường được sử dụng để điều trị ung thư phổi. Tuy nhiên, liều bức xạ cần thiết để loại bỏ hoàn toàn khối u khi bổ sung AVA thấp hơn nhiều so với khi không bổ sung.
Các thí nghiệm sâu hơn trên các tế bào ung thư phổi đã xác nhận rằng AVA gây ra sự gia tăng sản xuất hydro peroxide bởi các tế bào ung thư phổi tiếp xúc với bức xạ trong khi cùng một sự kết hợp giữa AVA cộng với các tế bào phổi bình thường được bảo vệ bức xạ. Khi sự kết hợp giữa bức xạ và AVA được tiêm cho những con chuột có khối u tạo ra lượng enzyme dồi dào để loại bỏ hydro peroxide, hầu như không có thêm lợi ích nào và các khối u ở những con chuột đó tiếp tục phát triển. Các nhà nghiên cứu kết luận rằng những phát hiện này chỉ ra rằng chính sự tăng cường hydrogen peroxide từ AVA đã giết chết các tế bào khối u sau khi xạ trị. Tế bào ung thư phổi không phải là loại tế bào ung thư duy nhất tỏ ra nhạy cảm hơn với phương pháp điều trị kết hợp. Các nhà nghiên cứu cũng phát hiện ra rằng AVA làm tăng khả năng tử vong do bức xạ của cả tế bào ung thư đầu, cổ và tế bào ung thư tuyến tụy. Dựa trên những kết quả này, hai thử nghiệm lâm sàng đang được tiến hành thử nghiệm sự kết hợp giữa AVA và xạ trị ở những người bị ung thư phổi và ung thư tuyến tụy. Ung thư tuyến tụy thường kháng lại điều trị bằng bức xạ. Thử nghiệm mới về bệnh ung thư tuyến tụy đang kiểm tra xem việc bổ sung AVA vào SBRT có thể cải thiện thời gian sống của những người mắc bệnh ung thư nguy hiểm này hay không.
Việc sử dụng AVA và các chất bắt chước SOD tương tự có thể vượt ra ngoài liệu pháp xạ trị. Các nghiên cứu ban đầu đã gợi ý rằng các hợp chất này có thể bảo vệ thận khỏi tác hại của thuốc hóa trị liệu cisplatinExit. Trong nghiên cứu như vậy, tất cả những người dùng đủ liều cisplatin đều mắc bệnh thận mãn tính. Nhưng không ai trong số những người có AVA mắc phải. Các nhà nghiên cứu cũng đang bắt đầu kiểm tra xem liệu sự kết hợp giữa các loại thuốc như AVA và bức xạ có thể nâng cao hiệu quả của thuốc ức chế điểm kiểm soát miễn dịch, một loại liệu pháp miễn dịch hay không. Ý tưởng cốt lõi là DNA của tế bào ung thư bị tổn thương do bức xạ có thể được nhận ra bởi các bộ phận của hệ thống miễn dịch thường phản ứng với mối đe dọa từ virus. Hệ thống miễn dịch sau đó sẽ coi các tế bào ung thư là mục tiêu. Các chất ức chế điểm kiểm soát sau đó sẽ ngăn chặn các cơ chế mà tế bào ung thư thường sử dụng để ức chế hệ thống miễn dịch và hy vọng là sẽ tăng cường phản ứng miễn dịch. Các nhà nghiên cứu đã thử nghiệm ý tưởng này chỉ với bức xạ. Tuy nhiên, ông nói thêm rằng việc kéo dài thời gian sản xuất hydro peroxide và gây tổn hại DNA bằng một hợp chất như AVA có khả năng làm cho chiến lược này hiệu quả hơn.
Từ khóa: xạ trị; avasopasem mangan;
– CMD –






