Bắt kịp theo tiến bộ của công nghệ, các nhà khoa học đã tiếp tục khám phá và phát triển các liệu pháp cải tiến nhằm ứng dụng hiệu quả và giảm thiểu tác hại trong quá trình cải thiện tỷ lệ kiểm soát ung thư và khả năng sống sót của bệnh nhân. Liệu pháp bắt neutron boron hay còn gọi là xạ trị kích hoạt boron bằng neutron (BNCT) đã được đưa ra từ nhiều thập kỷ trước như một phương pháp xạ trị tiên tiến và về lý thuyết, có thể là phương pháp điều trị lý tưởng cho nhiều loại ung thư. Phương pháp này được tiến hành bằng cách dược chất phóng xạ chứa boron vào cơ thể bệnh nhân. Dược chất phóng xạ sẽ tập hợp trong các tế bào khối u. Dưới tác động của việc chiếu xạ neutron nhiệt đến vị trí khối u, khi các neutron nhiệt bị 10B bắt giữ, sự phân hạch xảy ra, tạo ra hạt α và hạt nhân 7Li có thể “tiêu diệt” chính xác các tế bào khối u.
Xạ trị kích hoạt boron bằng neutron (Boron neutron capture therapy – BNCT) là phương pháp điều trị ung thư, đưa hợp chất chứa boron tập trung chọn lọc trong các tế bào khối u, sau đó chiếu xạ neutron. Các hạt neutron nhiệt gây phản ứng hạt nhân biến đồng vị bền 10B thành đồng vị phóng xạ 11B. Đồng vị phóng xạ 11B phân rã thành hai là hạt α (như hạt nhân của Helium-4) và đồng vị bền Lithium-7.
Các hạt này giải phóng năng lượng trong một phạm vi ngắn (<10 μm). Kích thước của một tế bào đơn lẻ là khoảng 10 μm; do đó, phản ứng bắt giữ neutron bo xảy ra trong một ô đơn lẻ. Về mặt lý thuyết, 10B có thể được tập hợp một cách chọn lọc trong các tế bào khối u ác tính; do đó, BNCT tiêu diệt có chọn lọc các tế bào khối u bằng hai hạt nặng (4He và 7Li) mà không gây ảnh hưởng đến mô lành xung quanh.
Phản ứng phân hạch: 10B + nth→ [11B]* → α + 7Li + 2,31 MeV
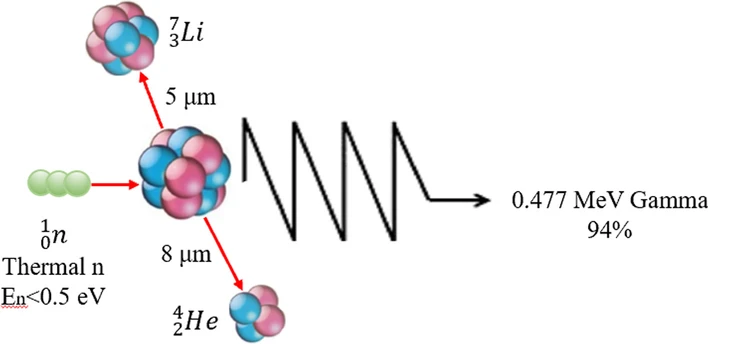
Phản ứng bắt neutron boron
Các yếu tố sinh học phóng xạ cơ bản của BNCT
Trong quá trình BNCT, có ba năng lượng ion hóa trực tiếp với các đặc điểm truyền năng lượng tuyến tính (LET) khác nhau được truyền đến khối u và các mô lành, như sau: (a) Các hạt α LET năng lượng cao (4He) và các ion 7Li được tạo ra; (b) Tia gamma LET năng lượng thấp được tạo ra bởi phản ứng bắt neutron của hydro: 1H + n = 2H + γ + 2,2 MeV; (c) Các proton LET năng lượng cao được tạo ra bởi sự tán xạ neutron nhanh và bắt neutron nhiệt bởi các nguyên tử nitơ: 14N + n = 14C + p + 580 keV. Ngay cả khi với liều lượng giống nhau, tác dụng sinh học của các hạt LET năng lượng cao và LET năng lượng thấp cũng sẽ khác nhau. Trong trường hợp với cùng liều lượng, các hạt LET năng lượng cao hơn tạo ra hiệu ứng sinh học mạnh hơn các hạt LET năng lượng thấp do mật độ ion hóa cao dọc theo quỹ đạo. Điều này thường được gọi là hiệu ứng sinh học tương đối và bằng tỷ số giữa liều hấp thụ của một nguồn bức xạ chuẩn (chẳng hạn như tia X) với liều hấp thụ của các nguồn bức xạ khác tạo ra cùng một hiệu ứng sinh học.
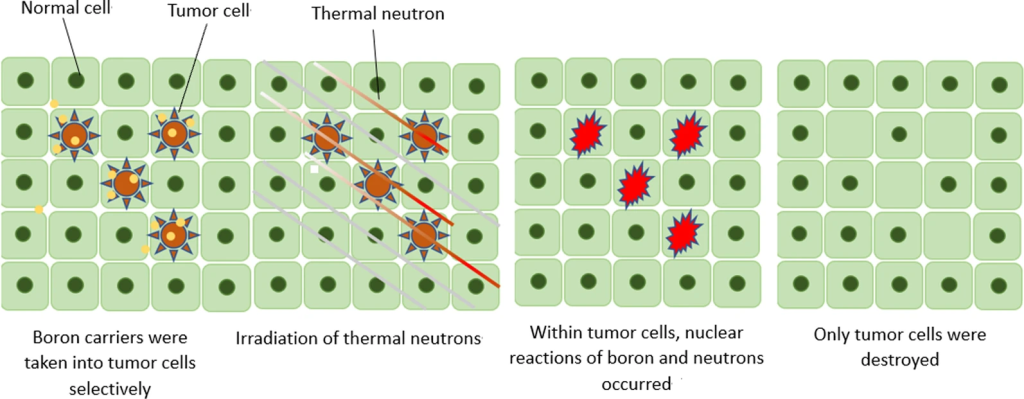
Cơ chế tiêu diệt chọn lọc tế bào khối u bằng liệu pháp bắt giữ nơtron bo
BNCT tiêu diệt tế bào khối u chủ yếu dựa vào hai điểm sau: 10B và neutron nhiệt. Nồng độ cao và sự phân phối chọn lọc của 10B đến các mô của khối u là những yếu tố quan trọng nhất để điều trị các khối u bằng BNCT. Để BNCT đạt được hiệu quả tối ưu, cần xem xét đến ba yếu tố quan trọng sau đây: (1) Nồng độ 10B trong các mô khối u phải là từ 20 – 35 μg 10B/g; (2) Tỷ lệ nồng độ 10B trong khối u/mô lành và tỷ lệ nồng độ 10B của khối u/trong máu lớn hơn 3 – 5; (3) Độc tính phải đủ thấp.
BPA (4-dihydroxy-borylphenylalanine) được coi là đại diện cho thế hệ đầu tiên của hợp chất chứa boron sử dụng trong phương pháp BNCT, đại diện của thế hệ thứ hai của hợp chất chứa boron là BSH (sulfahydryl borane) và thế hệ thứ ba của hợp chất chứa boron chủ yếu bao gồm nhóm boron bền hoặc gắn kết thông qua liên kết bền thủy phân. Đến nay đã có một số tác nhân thế hệ thứ ba đã được nghiên cứu, như các tác nhân antisense, polyethedral borane, carbohydrate, axit amin, liposome và gần đây, chất mang boron phổ biến nhất – boronophenylalanin (BPA) – được gắn nhãn flo-18 (F-BPA) đã được phát triển và ứng dụng thành công để theo dõi dược động học của BPA bằng công nghệ chụp cắt lớp phát xạ positron (PET), cho phép thu thập thông tin về khối u cũng như đánh giá sự tích tụ boron trong cả khối u và trong mô bình thường.
Do cơ chế hoạt động khác nhau, BPA chủ yếu nhắm vào các tế bào khối u đang tăng sinh và tạo ra nồng độ boron cao hơn, do đó BPA-BNCT gây tổn thương khối u lớn hơn và tác dụng phụ thấp hơn BSH-BNCT. Sự kết hợp giữa BPA và BSH có thể thu được sự phân bố đồng đều hơn của boron trong khối u và đạt được hiệu quả BNCT tốt hơn. Cải thiện việc sử dụng BPA và BSH, như dung dịch mannitol tiêm tĩnh mạch, siêu âm hội tụ hoặc sử dụng trực tiếp trong khối u qua phân phối tăng cường đối lưu, làm tăng đáng kể sự hấp thu BPA và BSH trong u não và cải thiện hiệu quả của BNCT. Với sự tiến bộ của PET, BPA gắn 18F có thể đưa ra trực quan sự phân bố 10B trong cơ thể con người thông qua hình ảnh PET, cung cấp hướng dẫn xây dựng cho việc lập và thực hiện kế hoạch xạ trị BNCT. Sau nhiều thập kỷ phát triển, hiện nay chỉ có BPA và BSH được sử dụng trong thực hành lâm sàng, trong đó BPA là chất mang bo được ưu tiên cho BNCT lâm sàng ở bệnh nhân u thần kinh đệm độ cao và u tái phát ở đầu và cổ. Thế hệ thứ hai của chất mang boron tuy chưa hoàn hảo, nhưng đã kéo dài sự sống của hàng triệu bệnh nhân và điểm mốc quan trọng trong sự phát triển của chất mang bo.
Nguồn neutron cho BNCT
Các neutron được tạo ra trong lò phản ứng hạt nhân có thể được phân loại là neutron nhiệt (En <0,5 eV), neutron trên nhiệt (0,5 eV <En <10 keV) và neutron nhanh (En> 10 keV). Nơtron nhiệt là nguồn nơtron quan trọng nhất trong BNCT, có thể tham gia vào phản ứng bắt neutron bo. Tuy nhiên, triển vọng với nguồn neutron này không khả quan vì chi phí cao, yêu cầu không gian lớn, khó trang bị và chi phí vận hành, bảo dưỡng cao. Do đó, BNCT hiện sử dụng chủ yếu bằng các máy gia tốc.
Hiện nay, trên thế giới có nhiều loại máy gia tốc phát neutron khác nhau, như máy gia tốc tuyến tính năng lượng thấp, Cyclotron năng lượng cao, máy gia tốc tuyến tính năng lượng cao và Synctron năng lượng cao đang được xem xét sử dụng cho BNCT. BNCT sử dụng máy gia tốc có nhiều ưu điểm hơn so với lò phản ứng như: Máy gia tốc có thể dễ dàng tắt khi không sử dụng; Quy trình cấp phép cho máy gia tốc đơn giản hơn; Việc lắp đặt và bảo trì máy gia tốc dễ dàng hơn; Hệ thống BNCT sử dụng máy gia tốc rẻ hơn so với chi phí lắp đặt hệ thống lò phản ứng trong/gần bệnh viện; Khối lượng của nguồn neutron do máy gia tốc tạo ra lớn hơn nhiều với lò phản ứng.
U thần kinh đệm ác tính
Nghiên cứu lâm sàng về BNCT sử dụng máy gia tốc đối với u thần kinh đệm ác tính ở Nhật Bản cho thấy thời gian sống thêm trung bình (MST) là 10,8–27,1 tháng. Kết quả tương đương với kết quả xạ trị thông thường. Dữ liệu lâm sàng cho thấy BNCT có hiệu quả như một điều trị bổ trợ cho u nguyên bào thần kinh đệm đa dạng mới được chẩn đoán sau phẫu thuật cắt bỏ. Mặc dù có rất ít khác biệt về thời gian sống sót giữa BNCT và xạ trị thông thường bằng temozolomide, nhưng kết quả đánh giá BNCT gần đây cho thấy hiệu quả BNCT có thể so sánh với kết quả tốt nhất của các phương pháp xạ trị liều cao.
Các khối u tái phát của vùng đầu và cổ
Nhóm bệnh nhân được điều trị BNCT lớn thứ hai là những bệnh nhân có khối u tái phát ở đầu và cổ đã trải qua phẫu thuật, hóa trị và xạ trị photon với liều đạt ngưỡng dung nạp của mô lành trong trường hợp không có lựa chọn điều trị khác. Ung thư đầu và cổ (HNC) chiếm khoảng 10% các loại ung thư và khoảng 90% trong số đó là ung thư biểu mô tế bào vảy (SCC). Các bệnh nhân có khối u tái phát ở đầu và cổ cho thấy đáp ứng tốt với BNCT theo Tiêu chí Đánh giá Đáp ứng cho các khối u rắn, các báo cáo về tỷ lệ đáp ứng dao động từ 61 đến 100%. Mặc dù số lượng bệnh nhân có khối u tái phát ở đầu và cổ được điều trị bằng BNCT tương đối ít, nhưng hiệu quả lâm sang thu được lại rất cao. Thời gian sống thêm trung bình là 33,6 tháng với tỷ lệ đáp ứng lên đến 85%.
Các khối u ác tính trên da
Các khối u ác tính trên da là các khối u ác tính phát sinh từ các tế bào hắc tố, tức là các tế bào sắc tố và là loại phổ biến nhất đối với các khối u ác tính. Từ năm 2003 đến năm 2014, tám bệnh nhân bị u ác tính trên da đã được điều trị bằng BNCT tại Nhật Bản. Tất cả các tổn thương dần dần thuyên giảm trong vòng 01 năm. Tỷ lệ đáp ứng hoàn toàn và không có biến chứng nào chứng minh BNCT có thể là phương thức điều trị đầy tiềm năng đối với các khối u ác tính ở da. Đánh gia trên 32 bệnh nhân bị u hắc tố da được điều trị bằng BNCT sử dụng BPA làm chất mang bo, tỷ lệ đáp ứng hoàn chỉnh lên tới 78%.
Như vậy, rõ ràng BNCT là phương pháp điều trị kết hợp vật lý hạt nhân, hóa học, sinh học, y học và các yếu tố khác. Sau nhiều thập kỷ nghiên cứu và phát triển lâm sàng, BNCT đã trở thành một công nghệ điều trị ung thư hiệu quả cao. Mặc dù hiện tại BNCT chưa được phổ biến rộng rãi, nhưng BNCT sẽ là một cột mốc quan trọng của điều trị ung thư trong tương lai gần.
Từ khóa: BNCT; xạ trị; neutron;
– CMD&DND –