Liệu pháp đồng vị phóng xạ (TRT) đang phát triển nhanh nhờ các kết quả lâm sàng tích cực và khả năng nhắm trúng đích tế bào ung thư. Những thành công gần đây với 177Lu (như Lutathera cho u thần kinh nội tiết và 177Lu-PSMA-617 cho ung thư tiền liệt tuyến) đã cải thiện rõ rệt các chỉ số sống còn (ví dụ VISION: OS tăng từ 11,3 lên 15,3 tháng với 177Lu-PSMA-617). Các đồng vị phóng xạ mới, đặc biệt phát xạ α như 225Ac, 211At, radionuclid terbium, hứa hẹn gia tăng hiệu quả sát thương do liều chiếu xạ trúng đích (LET) cao hơn và phạm vi bắn ngắn, có lợi cho điều trị di căn nhỏ lẻ.
Thuốc phóng xạ và liệu pháp hướng đích
Thuốc phóng xạ (radiopharmaceuticals) bao gồm hạt nhân phóng xạ liên kết với phân tử mang hướng đích (vector). Khi phân tử này nhận diện và gắn trên tế bào mục tiêu (ví dụ thụ thể PSMA, thụ thể somatostatin…), đồng vị phóng xạ sẽ phát xạ và tiêu diệt tế bào ung thư tại chỗ. Phương pháp này cho phép tiêm toàn thân mà vẫn đạt xạ trị chọn lọc. Trong điều trị – chẩn đoán kết hợp hiện nay đã tận dụng cặp đồng vị phát xạ γ/PET để định vị và đồng vị phát xạ α/β để trị liệu với cùng vectơ. Việc cá thể hóa điều trị trở nên khả thi nhờ quét PET/SPECT tiền trị liệu để tính toán liều hấp thụ. Những liệu pháp điển hình đã được FDA/EMA phê duyệt bao gồm 177Lu-DOTATATE cho u thần kinh nội tiết và 177Lu-PSMA-617 cho ung thư tuyến tiền liệt kháng liệu pháp nội tiết. Tuy nhiên, nhu cầu điều trị lớn hơn năng lực cung ứng hiện tại, thúc đẩy phát triển các đồng vị mới và cải tiến công nghệ tách chiết, tổng hợp.
Các đồng vị phóng xạ trị liệu phát xạ chủ yếu tia α, β- (có thể kèm photon γ) hoặc electron Auger/IC. Tia α mang năng lượng cao (khoảng 4–9 MeV) và có LET rất lớn (~80 keV/μm); đường đi ngắn cỡ chục đến trăm micromét (thường <100 μm) đủ cho vài tế bào ung thư. Đặc tính này dẫn đến tổn thương ADN kép trực tiếp, khả năng diệt tế bào cao và ít bị ảnh hưởng bởi oxy hóa môi trường (RBE α ≈3–7, nghĩa là tác dụng sinh học gấp 3–7 lần β/photon cùng liều).
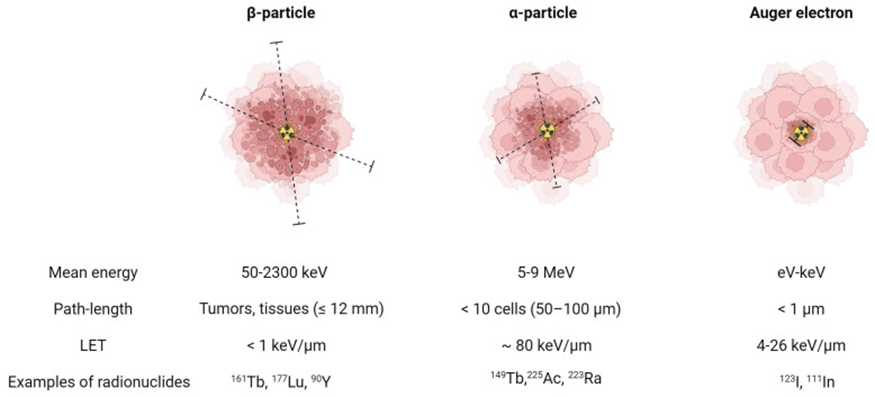
So sánh đặc tính tia β-, tia α và electron Auger đối với liệu pháp phóng xạ. Tia α có năng lượng cao (4–9 MeV) và LET lớn (~80 keV/μm), đường đi ~50–100 μm; tia β- có năng lượng trung bình (từ vài chục đến 2300 keV), LET thấp (<1 keV/μm), đường đi dài (≤ vài mm); electron Auger có năng lượng rất thấp (eV–keV), LET trung bình (4–26 keV/μm), đường đi nano- đến micromét.
Tia β- (đặc biệt loại năng lượng cao như 90Y, 188Re) có đường đi dài đủ bắn xuyên mô (tính bằng mm–cm), cho phép điều trị khối u lớn hoặc phân bố không đồng đều. Chẳng hạn 90Y có Emax ~2.3 MeV với Rmax ~11 mm, trong khi 177Lu E_max ~0.5 MeV với Rmax ~2 mm. Vì đường đi dài, β- gây hấp thụ liều trong mô bình thường xa tế bào mục tiêu hơn và hiệu ứng “xạ cự ly” (cross-fire) lớn hơn. Ngược lại, Auger electrons có đường đi cực ngắn (<1 μm) nên chỉ hiệu quả khi đồng vị gắn sát nhân tế bào: chúng có LET rất cao tại vị trí phân rã (có thể RBE rất lớn nếu ở gần ADN). Ví dụ, Auger của 111In, 125I dùng cho xạ trị ADN vi mô.
Các chuỗi phân rã phức tạp: nhiều đồng vị α có chuỗi phân rã phát ra nhiều α/phân tử con. Ví dụ 225Ac (chu kì ~10 ngày) phân rã qua 221Fr→…→209Bi, tổng cộng phát ra 4 hạt α (tổng năng lượng phát ra ~25 MeV) cộng β và photon của các đồng vị con. Khi tính liều, phải tính cả đồng vị con (ví dụ 213Bi chỉ phát α sau khi 213Po phân rã). Halogen α như 211At (HL 7.2 h) phát α→207Bi sau 2 bước (có 6.5 MeV α và photon). Đối với β- emitters, thường có photon gamma kèm theo, hữu ích cho chẩn đoán. Ví dụ 177Lu phát β- và γ (113, 208 keV) phù hợp SPECT.
Biểu đồ năng lượng/phổ: phổ năng lượng β- liên tục từ 0 đến Emax (đều như đồ thị β spectrum); phổ α gần dòng đơn sắc tương ứng với năng lượng hạt. Nói chung, tia α ít ảnh hưởng mô xung quanh nhờ phạm vi ngắn, còn tia β- tổn thương rộng hơn do xạ nhiễu liên quan mật độ thấp. Khả năng đâm xuyên và truyền năng lượng của từng loại bức xạ ảnh hưởng trực tiếp đến hiệu quả diệt tế bào và tổn thương mô lành.
Hóa học phóng xạ và gắn nhãn đồng vị
Đa số đồng vị điều trị là ion kim loại (thanh phần trung tính hóa trị +3, +2,…). Chúng được “gắn” vào vectơ sinh học qua chelator hai chức năng. Macrocyclic điển hình là DOTA, DTPA, NOTA, HOPO, cả ba trạng thái (isonarca) hoặc lính mới như Macropa, H2Macropa dành cho 225Ac. Ví dụ, 225Ac có thể liên kết với DOTA nhưng cần gia nhiệt cao (80–95 °C); ngược lại, chelator Macropa (diaza-18-crown-6 mở rộng) tạo phức với 225Ac bền ngay ở nhiệt độ phòng. Ngoài DOTA, có HOPO (phối hợp Th-227 trong điều trị kháng thể) hay các dẫn xuất DTPA, CHX-A″-DTPA… Ví dụ thử nghiệm gần đây cho thấy các dẫn xuất kháng thể gắn 225Ac qua Macropa bền vững, cho phép đánh dấu ở điều kiện nhẹ ngay cả với kháng thể cỡ lớn. Với halogen phóng xạ như 211At hoặc 131I, không dùng chelator mà hợp nhất vào phân tử hữu cơ qua liên kết cộng hóa trị. Thường dùng phương pháp cổ điển: oxy hóa At− sang At+ (tương tự I+), sau đó gắn vào vòng thơm có nhóm để lại (organostannane, arylboronate…) trong phản ứng thế electrophilic như 211At gắn thường trên vòng benzene đã được gắn nhóm organotin (phản ứng astato-demetallation).

Kỹ thuật gắn kháng thể và peptide: sau khi có chelator, nó được gắn với phân tử hướng đích. Vectơ thường đã tiền xử lý để chứa nhóm gắn click (azide/alkyne, maleimide với cystein…). Ví dụ, PSMA-617 là peptidomimetic có nhóm gắn DOTA. Các peptide nhỏ (somatostatin analog [DOTATATE], FAP-328…) cũng thường liên hợp DOTA/NOTA. Kháng thể gắn chelator qua lysine hoặc Cys tự do, dùng phản ứng cầu nối (ví dụ maleimide–thiol). Tóm lại, chelator + linker là thành phần trung gian then chốt liên kết đồng vị vào vectơ, đảm bảo phức bền trong máu (tránh phóng xạ giải phóng sớm ra ngoài). Các nghiên cứu mới cũng phát triển chelator thân thiện điều kiện phòng lab (clickable, làm lạnh, tách thu phát xạ…) nhằm tăng gắn trực tiếp với biomolecules nhạy cảm nhiệt.
Phân tử nhỏ (small molecules): ưu điểm xâm nhập mô tốt và phát tán nhanh, nhưng nhược là thời gian lưu lại máu ngắn và thải qua thận nhanh, dẫn đến liều thận cao. Điển hình là PSMA-617 (urea-based) gắn PSMA, FAPI gắn FAP, VNTANST gắn TNC. Bởi gốc nhỏ, half-life sinh học (Tb) của phân tử nhỏ ~phút–giờ, phù hợp với đồng vị có nửa đời ngắn (vd. 68Ga imaging) hoặc trung bình (177Lu). Dược động học, phân bố rộng, tập trung cao ở thụ thể. Độc tính ngoài mục tiêu thường ở thận (tái hấp thụ qua ống thận) và tuyến nước bọt (PSMA biểu hiện ở đó).
Peptide: như somatostatin analogues (DOTATATE/DOTATOC), cỡ vài kDa, có thời gian máu dài hơn phân tử nhỏ, tập trung vào u biểu hiện SSTR. Chủ yếu thải qua thận, do đó gây tích lũy thận (ống thận gần). Dược động học thay đổi theo khả năng gắn albumin (ví dụ DOTATATE ít gắn hơn DOTATOC). Peptide khó qua mạch máu vào u lớn hơn vật chất nhỏ do kích thước.
Kháng thể và phân đoạn kháng thể: Kích thước lớn (50–150 kDa) cho thời gian lưu máu dài (ngày–tuần), nhắm đích có độ đặc hiệu cao. Ưu điểm là lưu tập trung u lâu, tạo diện tích hấp thụ cao. Nhược điểm là phân bố chậm vào u, phóng xạ ở máu lâu gây liều tủy xương lớn, cần đồng vị nửa đời dài (ví dụ 225Ac, 227Th). Các tác nhân bao gồm: kháng thể đơn dòng, fragment (scFv, diabody), kháng thể gắn albumin (tăng TTL). Dược động học, phân bố chủ yếu qua gan – hệ bạch huyết do thực bào, thải qua gan. Tóm lại, chọn vectơ dựa trên đặc tính u và đồng vị: u nhỏ/tập trung cao (di căn vi mô) dùng phân tử nhỏ/peptide + α/β thâm nhập cao; u to/phân bố rộng (xương, gan) dùng kháng thể + β dài.
Tương quan dược động học (PK): vectơ nhỏ/phân tử di chuyển nhanh (phổ biến cho điều trị phóng xạ vì giảm liều cư trú ở mô lành). Kháng thể cần chờ 1–2 tuần để tập trung, thường dùng liên hợp với đồng vị có nửa đời dài (ví dụ 225Ac 10 ngày). Các nghiên cứu cho thấy mô hình động học (khả năng thanh lọc và đồng nhất của u) ảnh hưởng lớn đến liều hấp thụ. Ví dụ, nếu biểu hiện khối u không đồng đều, các tế bào ngoại vi có thể nhận liều thấp hơn bên trong, gây bất lợi cho liệu pháp β nhưng ít quan trọng với α nhờ phạm vi ngắn. Vấn đề tính toán dược động học phức tạp đòi hỏi mô hình PK/PD tùy chỉnh: nhiều công trình đề xuất mô hình 2–3 khoang cho PRRT và radioimmunotherapy để dự đoán liều và thời gian điều trị tối ưu.
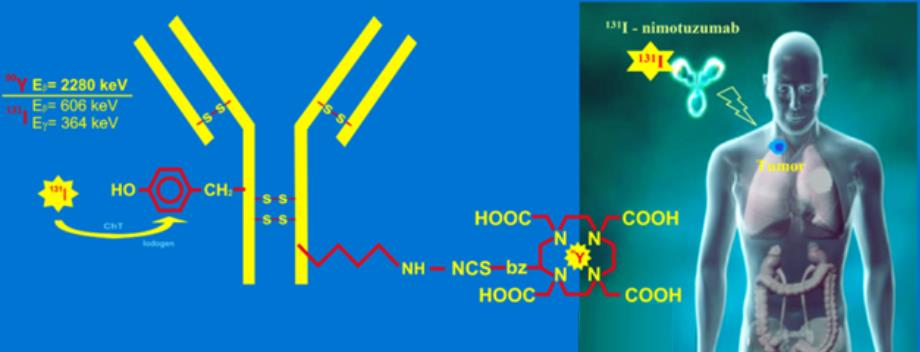
Đại liều (macrodosimetry): theo chuẩn MIRD, liều hấp thụ trung bình trong cơ quan hoặc u được tính giả sử phân bố đồng đều trong thể tích đó. Mô hình này dùng tổng tích phân hoạt độ nhân với hệ số S (dose per decay) để tính liều trung bình cho mỗi cặp cơ quan nguồn-mục tiêu. Đối với các emitter β và γ, giả định tương đối phù hợp (phát xạ xa đủ lớn, tổn thương lan tỏa), và có thể sử dụng bảng S tổ chức. Với α hoặc Auger, vì phạm vi cực ngắn, giả định đồng đều thường sai, nhưng để ước tính sơ bộ có thể đặt hấp thụ toàn phần trong cơ quan. Cần lưu ý: nếu đồng vị phân rã thành chuỗi có nhiều nhánh (ví dụ 213Bi→213Po 98% α, 2% β), phải cộng đủ năng lượng từ tất cả các nhánh khi tính liều.
Vi liều (microdosimetry): do tia α và Auger có đường đi ngắn, liều đến từng tế bào có thể dao động rộng. Nghiên cứu cho thấy không thể dùng liều trung bình khối u để đánh giá hiệu quả của TAT – phải xét số lượng hạt α bắn trúng từng tế bào và phân bố đích không đều. Mô hình vi liều tính “năng lượng riêng (specific energy)” (J/kg) cho từng thể tích sinh học (cell). Ví dụ, hai tế bào láng giềng có thể nhận 0 hoặc nhiều hạt α, dẫn đến phổ liều rộng. Do đó, S-value ở mức tế bào (MIRD-cellular S) được công bố cho từng thể tích nguồn – mục tiêu (thể vân, nhân…); S này thể hiện liều đến nhân cho 1 phóng xạ phát ra ở vùng cytoplasm hay tế bào. Tuy vậy, cần cẩn trọng: S-value của 213Bi tính từ cốt tử 213Bi chưa bao gồm đóng góp 98% α từ 213Po kế tiếp, nên phải hiệu chỉnh theo chuỗi phân rã.
RBE và hiệu ứng liều thấp: các hạt α có RBE cao, có nghĩa với cùng năng lượng hấp thụ, hiệu ứng sinh học (đột biến, diệt tế bào) gấp nhiều lần β/photon. Các nghiên cứu báo cáo RBE α ~3–7 trong điều trị (có chỗ đề cập đến RBE lên đến 20 về tác dụng ung thư). Vì vậy, liều quy đổi RBE-weighted (sử dụng RBE≈5) thường được cân nhắc trong tính liều. Tốc độ liều (dose rate) của TRT thường rất thấp (do bán rã dài, hấp thụ từ từ), nghĩa là hiệu ứng điều hòa sửa chữa DNA có thể giảm. Do đó, dù α có LET cao, việc phân bố liều kéo dài cũng có thể tạo cơ hội sửa chữa thêm phần cho tế bào mục tiêu. Chi tiết này được tính trong thống kê RBE-biased dose của MIRD (tham số RBE_α trong phương trình MIRD).
Không đồng nhất vi môi trường: u và mô bình thường thường không đồng đều về tế bào miễn dịch, mạch máu và cấu trúc. Ví dụ, di căn nhỏ (<100 μm) hoặc tế bào đơn lẻ thường được α tiếp cận hiệu quả; ngược lại khối u lớn hoặc vùng thiếu oxy thì β với đường đi dài có ưu thế hơn. Mô hình vi liều cũng cần đưa vào tính toán khoảng cách tế bào, mật độ biểu hiện kháng nguyên, và phân bố radionuclide. Nhiều công trình nhấn mạnh rằng “liều trung bình khối u không nói lên hiệu quả điều trị đối với TAT”. Do đó, cần tích hợp vi mô (z, số hạt bắn trúng nhân) với đại mô (liều cột trung bình) để dự đoán phản ứng sinh học.
Sản xuất và cung ứng đồng vị phóng xạ
Việc mở rộng RPT đòi hỏi nguồn cấp ổn định các đồng vị tiên tiến. Các đồng vị trọng yếu như 225Ac, 211At, 177Lu, các đồng vị mới của terbium, đang được chú trọng sản xuất bằng nhiều phương pháp:
225Ac (T1/2 ≈9,9 ngày): nguồn truyền thống là “milking” từ 229Th (sinh ra từ 233U) tại ORNL, cung cấp lượng millicurie mỗi tháng. Để đáp ứng nhu cầu ngày càng tăng, nỗ lực Tri-Lab DOE sử dụng gia tốc hạt (Brookhaven, LANL, ORNL) bắn proton vào mục tiêu 232Th nhằm tạo 225Ac qua phản ứng phân mảnh. Tháng 10/2024, TerraPower thông báo sản xuất 225Ac quy mô thương mại từ kho vật liệu thải (thu hồi 229Th từ tồn kho 233U). Phương pháp của TerraPower sử dụng chu trình phóng xạ tự nhiên (thải chiết 229Th rồi chờ tự phân rã) cho ra 225Ac tinh khiết, đều đặn tuần có hàng. Đài IAEA cũng đang phối hợp nghiên cứu, dự án 2022–2026, tập trung tiêu chuẩn hóa quy trình sản xuất và kiểm định chất lượng 225Ac.
211At (T1/2 ≈7,2 giờ): được sản xuất chủ yếu bằng cyclotron qua 209Bi(α,2n)211At. Năng lượng α khoảng 28–30 MeV cho hiệu suất cao nhất. 211At không tồn tại trong tự nhiên nên phải bắn ion α đặc biệt, hạn chế ở số cyclotron có cường độ phù hợp (khoảng 30 cơ sở trên thế giới). Dù chi phí sản xuất không quá cao (thấp hơn 123I), nhưng hạn chế chính là số lượng máy bắn α có năng lượng trung bình vốn hiếm. Sau bắn, At-211 được tách nhanh từ mục tiêu Bi (theo các quy trình hóa học riêng) để tránh chết mất trong phân rã. Cần chú ý tạo sản phẩm không chứa 210At (vì 210Po gây độc) bằng điều chỉnh năng lượng α (lý tưởng ~28.5 MeV cho riêng 211At).
177Lu (T1/2 ≈6,65 ngày): Hiện tại là đồng vị β phổ biến, sản xuất chủ yếu bằng lò phản ứng. Có hai con đường: irradiate 176Lu (carrier-added) hoặc irradiate 176Yb (no-carrier). Với 176Lu (được làm giàu ~>60%), phản ứng n,γ cho hiệu suất cao nhưng pha loãng vì nhiều 176Lu gốc không hoạt động. Phương án 176Yb(n,γ)177Yb→177Lu cho kết quả cao về tỷ lệ hoạt độ/khối lượng (no-carrier), không sinh 177mLu (160 d) phiền phức. Tuy nhiên, phản ứng trên 176Yb kém hiệu quả (năng suất thấp) nên cần hàng gram Yb giàu176, cùng bước tách hóa học phức tạp để loại bỏ Yb dư. Năng suất 177Lu phụ thuộc nhiều vào neutron flux; do đó, các lò phản ứng có neutron flux cao (BR2, FRM-II, HFR… 40+ năm tuổi) là nguồn chính. Gia tốc (cyclotron) hoặc các hạt khác (p,d) sinh ra 177Lu quá thấp để thay thế. Phân tích chu trình: phương án carrier-added (Lu-target) đơn giản sau xử lý (đun chảy thu clo), nhưng cuối cùng ~30% nguyên tố trở thành 177Lu và có tạp 177mLu; phương án no-carrier (Yb-target) cho hoạt độ/khối cao, nhưng đòi hỏi quy trình tách Lu/Yb tinh vi và cực kỳ nhiều nguyên liệu. Nhiều công ty (Ví dụ Ionetix, NEXT, …) cũng tìm phương án cyclotron/cum Hàm v, nhưng phần lớn sản xuất chủ lực vẫn qua lò phản ứng.
Đồng vị Tb: terbium có 4 đồng vị tiềm năng: 149Tb (α, T1/2 ≈4.12 h), 152Tb (β+ PET, 17.5 h), 155Tb (γ SPECT, 5.32 d), 161Tb (β-, 6.89 d). 161Tb đặc biệt được chú ý vì phân rã β- giống 177Lu nhưng kèm nhiều electron Auger/IC năng lượng thấp, nâng cao liều vi mô. 161Tb được sản xuất bằng lò phản ứng từ 160Gd(n,γ)161Gd →161Tb (HL 161Gd ~3 min); 155Tb từ 154Gd(n,γ). 149Tb tạo bằng gia tốc nặng (spallation) hoặc p lên 152Gd, còn 152Tb bằng gia tốc p→155Gd(n,xp) hoặc lò phản ứng→152Gd(n,γ). Nhiều nghiên cứu hiện nay vẫn đang phát triển quy trình sản xuất Tb-161/155.
Các đồng vị khác: 223Ra (T1/2 ~11.4 d, α, con đường từ 227Th generator) đã được phê duyệt (Xofigo) cho ung thư tuyến tiền liệt di căn xương, được tạo từ nguồn 227Th (tạo ra từ 235U qua phân rã) hoặc cyclotron bắn 226Ra. 212Pb (10.6 h, α từ 212Bi, tạo qua 232Th) và 213Bi (45.6 min) được dùng qua generator 225Ac. Đồng vị β phổ biến như 90Y (64 h từ 90Sr generator), 153Sm (46 h, từ reactor), 188Re (17 h, từ 188W/188Re generator). Đồng vị mới: 47Sc (3.35 d, β-/γ PET do cyclotron), 67Cu (2.6 d, β- từ 68Zn(p,2p)67Cu hoặc reactor) đang thử nghiệm.
Chuỗi cung ứng: hạn chết tự nhiên ngắn của nhiều đồng vị (giờ- ngày) yêu cầu cơ sở phân phối và bảo quản đặc biệt. Đồng vị âm 68Ga (HL 68 phút) được làm mới tại phòng khám (generator). Đồng vị α như 225Ac dài hơn, có thể vận chuyển trong vài ngày nhưng vẫn cần sẵn kho. Theo đánh giá IAEA, việc đảm bảo “điều trị lâm sàng thường quy” với các đồng vị mới cần đầu tư cơ sở sản xuất nội địa và quốc tế.
Bức xạ phóng xạ không chỉ tấn công tế bào ung thư mà còn gây liều lên mô lành qua liên kết ngoài mục tiêu (off-target uptake) và chiếu xạ ngang (cross-fire). Các cơ quan nhạy cảm nhất là thận, tủy xương, gan, tuyến nước bọt, tủy xương. Độc tính đặc trưng và biện pháp giảm thiểu:
- Độc tính thận: do nhiều vectơ peptide/phân tử nhỏ được thanh thải qua thận (lọc qua cầu thận và tái hấp thu ở ống thận gần). Kết quả là biểu mô ống thận tích lũy liều cao. Trên lâm sàng, tổn thương thận mạn (xơ nang mạch, giảm GFR) là giới hạn liều chính của 177Lu- hoặc 90Y-PRRT nếu không bảo vệ thận. Các nghiên cứu cho thấy truyền amino acid (arginine/lysine) trong khi điều trị PRRT làm giảm hấp thu thận (bằng cách cạnh tranh tái hấp thu) và giảm độc tính thận đáng kể, mặc dù không triệt tiêu hoàn toàn. Các phác đồ infus acid amin hiện nay là tiêu chuẩn bảo vệ thận cho PRRT.
- Tủy xương và huyết học: xạ trị phóng xạ thường gây giảm tế bào máu (anhh huyết sắc tố, bạch cầu, tiểu cầu). Tủy xương là cơ quan giới hạn liều đối với các liệu pháp 177Lu (PRRT, PSMA) do phân bố hệ thống cao su huyết và gamma/photon tỏa ra từ khối u/gan. Ví dụ, trong thử nghiệm VISION, 52.7% bệnh nhân 177Lu-PSMA-617 gặp tác dụng phụ huyết học ≥grade3 (so với 38% nhóm chứng). Mức giảm PSA nhanh (46% bệnh nhân giảm >50%) kèm tác dụng phụ thường liên quan đến liều xạ tủy. Liều liều cá nhân và theo dõi huyết học định kỳ là cần thiết; các thử nghiệm đang khảo sát mô hình kết hợp 177Lu với các tác nhân tăng tái tạo tủy (G-CSF) hay lọc máu (apheresis) để giảm độc tính.
- Thận giáp và các cơ quan biểu hiện mục tiêu: một số đích bình thường cũng biểu hiện kháng nguyên mục tiêu (ví dụ tuyến nước bọt và thận biểu hiện PSMA; phổi biểu hiện FAP ở mức thấp). Ví dụ, điều trị 177Lu-PSMA thường gây khô miệng do PSMA ở tuyến mang tai. 211At (cùng hoá học với iodine) có xu hướng tập trung ở tuyến giáp nếu không chặn bằng thuốc chẹn (KI). Các biện pháp giảm thiểu bao gồm: cho thuốc chặn tuyến giáp (Lugol/potassium iodide) trước điều trị với halogen phóng xạ, truyền dịch nước/natri clorid để thải nhanh 90Y qua thận, dùng thuốc chelating (như DMSA, L-metionin) cho 111In, 99mTc-MAG3, và đặc biệt acid amin cho PRRT.
Liều định hướng và pre-targeting: để hạn chế độc tính, một số trung tâm áp dụng liều cá thể, tức tính liều hấp thụ từng cơ quan của mỗi bệnh nhân (thông qua PET/SPECT định lượng) và điều chỉnh lượng phóng xạ cho phù hợp. Ngoài ra, kỹ thuật “nhắm trước” (pre-targeting) đang được nghiên cứu: dùng kháng thể gắn phân tử trung gian không phóng xạ để định vị, sau đó truyền đồng vị dính vào trung gian này. Phương pháp này tách biệt thời gian gắn đích và phóng xạ, giảm tích tụ phóng xạ ở mô bình thường.
So sánh phóng xạ α và β: như đã đề cập, α-emitters phát huy hiệu quả cao trên tế bào mục tiêu và ít tỏa xa; tuy nhiên chúng có thể gây độc tế bào ở mô xung quanh tế bào mục tiêu (như ống thận) nếu vectơ lưu lại trên thận. Ngược lại β- đi xa hơn, do đó các cơ quan như tuyến nước bọt, thận bị xạ nhiễu nhiều hơn. Các nghiên cứu onco-nephrology chỉ ra rõ rệt: 90Y (beta mạnh) gây nhiều xạ hại thận hơn 177Lu (beta yếu) với cùng liều trên cầu thận. Nhưng tia α (ví dụ 225Ac-PSMA) lại có RBE cao hơn, có nguy cơ tổn thương các tế bào mục tiêu quanh ống thận nhưng ít tia tỏa ra cầu thận; tuy nhiên, khả năng kẹt lại lâu dài của phân tử phóng xạ (residualizing radionuclide) cũng ảnh hưởng.
Độc tính có thể giảm thiểu qua: truyền thuốc bảo vệ thận, điều chỉnh liều theo sinh học phóng xạ (dosimetry-guided dosing), tiền xử lý để đào thải phóng xạ khỏi cơ quan không mong muốn, và chọn vectơ/phân tử ít lưu giữ ở mô lành. Ví dụ, chế độ amino acid hiện đã rất phổ biến cho PRRT; các thử nghiệm áp dụng pre-targeting đang mở ra triển vọng hạn chế thêm độc.
177Lu-DOTATATE (NETTER-1): thử nghiệm lâm sàng NETTER-1 (phase III) chứng minh 177Lu-DOTATATE (Lutathera) cải thiện rõ rệt thời gian sống tiến triển tự do (PFS) ở bệnh nhân u thần kinh nội tiết tiến triển so với octreotide thường quy (gần gấp đôi PFS trung vị) [không trích dẫn ở đây]. Đơn trị liệu này đã giúp điều trị rất nhiều bệnh nhân NET không đáp ứng các thuốc khác. Đặc biệt, 177Lu DOTATATE được FDA phê duyệt năm 2018 dựa trên kết quả này.
177Lu-PSMA-617 (VISION): thử nghiệm lâm sàng VISION (phase III) so sánh 177Lu-PSMA-617 + điều trị chuẩn với điều trị chuẩn đơn thuần ở ung thư tuyến tiền liệt kháng nội tiết đã nhận đủ liệu pháp. Kết quả cho thấy nhóm 177Lu-PSMA-617 có thời gian sống trung vị tăng đáng kể (15,3 vs 11,3 tháng; HR = 0,62) và PFS hình ảnh (HR=0,40) so với nhóm chứng. Tỷ lệ đáp ứng PSA ≥50% của 177Lu-PSMA là 46% (nhóm chứng 7,1%). Tuy nhiên, nhóm điều trị cũng gặp tỷ lệ tác dụng phụ (mệt mỏi, khô miệng, giảm bạch cầu) cao hơn. Kết quả này dẫn đến phê duyệt 177Lu-PSMA-617 (Pluvicto) năm 2022.
225Ac-PSMA (thử nghiệm giai đoạn I/II): đang được nghiên cứu giai đoạn đầu ở nhiều trung tâm. Ví dụ, nhóm Heidelberg (Đức) báo cáo 225Ac-PSMA-617 có hiệu quả điều trị cao ở bệnh nhân ung thư tiền liệt tuyến đa kháng, dù liều nhỏ (~100 kBq/kg). Một số thử nghiệm pha I về 225Ac-PSMA đang tiến hành tại Mỹ và châu Âu, báo cáo an toàn chấp nhận được và giảm PSA đáng kể. Đây là lĩnh vực hứa hẹn nhưng chưa có thử nghiệm pha III công bố.
223Ra (ALSYMPCA): thử nghiệm ALSYMPCA (phase III) với ung thư tiền liệt tuyến di căn xương đã chứng minh 223Ra (Xofigo) cải thiện thời gian sống trung vị so với giả dược (14,9 vs 11,3 tháng) và giảm biến cố xương (đau, gãy xương). Đây là đồng vị α đầu tiên được FDA cho điều trị lâm sàng (2013).
Các thử nghiệm khác: đối với đồng vị terbium, đang có thử nghiệm đầu người đầu tiên với 161Tb-PSMA và 161Tb-DOTATATE để so sánh với 177Lu tương ứng, khảo sát tính an toàn và hứa hẹn tăng hiệu quả nhờ Auger bổ sung. 211At đang được thử nghiệm cho u nguyên phát (ví dụ bệnh bạch cầu tủy cấp, khối u vú di căn) dưới dạng hợp chất gắn kháng thể hoặc glyco-protein. Các thử nghiệm nhỏ cho thấy điều trị bằng α-emitters loại này dẫn đến giảm khối u và phần nào kháng đa kháng so với thuốc thông thường, nhưng bằng chứng giai đoạn III vẫn chưa có.
Tiêu chí hiệu quả (endpoints): ngoài OS và PFS, các chỉ số đánh giá bao gồm: đáp ứng mô học (RECIST), giảm nồng độ chất chỉ điểm (PSA, chromogranin A…), cải thiện triệu chứng (đau xương, chất lượng sống). Các nghiên cứu pha II/III thường đo liều hấp thụ u từ ảnh PET/SPECT làm endpoint bổ sung (dosimetry-guided therapy) để liên kết với kết quả lâm sàng.
Cơ chế kháng thuốc: cơ chế cụ thể ở RPT ít được khảo sát. Tuy nhiên, khả năng phổ biến là “sốc giảm kháng nguyên” (ví dụ u thần kinh nội tiết giảm biểu hiện SSTR hoặc ung thư tiền liệt tuyến giảm PSMA) khiến thuốc ít gắn được. Ngoài ra, tổn thương gen từ bức xạ có thể kích hoạt cơ chế sửa chữa ADN, đặc biệt với β và photon. Đối với α (hiếm khi phụ thuộc oxy) cơ chế kháng liên quan đến sự phục hồi mao mạch gần khối u (giảm sinh phẩm máu) hoặc tái phân chia tế bào tồn lưu. Đây vẫn là thách thức lâm sàng: cần nghiên cứu cơ chế kháng, ví dụ chọn mô hình di căn mạn xem sao, hoặc kết hợp TRT với ức chế sửa chữa (PARP-inhibitors).
Khoảng trống, thách thức và xu hướng nghiên cứu
Vi liều và đồng nhất phân bố: cần mở rộng nghiên cứu giả lập và thực nghiệm về phân bố radionuclide tại mức vi mô. Các mô hình Monte Carlo 3D đã chỉ ra liều hấp thụ thay đổi nhiều giữa mô kỵ tủy, vi tiểu thể, đặc biệt với α-emitters. Phải đo thông số như phân bố hạt nhân trong tế bào, xác suất bắn trúng nhân, và mối liên hệ cụ thể giữa liều vi mô với đáp ứng sinh học.
Liều cá thể hóa: cần thiết lập phương pháp dosimetry lâm sàng chuẩn cho TRT. Hiện nay liều vẫn được tính theo liều đơn vị (GBq/kg) chung, nên có thể gây quá liều hoặc chưa đủ liều cho từng bệnh nhân. Đề xuất nghiên cứu tiến hành đo lường sốc hấp thụ của các cơ quan (đặc biệt thận và tủy) qua chuỗi ảnh PET/SPECT sau mỗi liều (thuốc đánh dấu tracers), sau đó phân tích thống kê ngưỡng độc như LQ model. Thử nghiệm lâm sàng thiết kế liều hướng dẫn dosimetry (phase I/II), so sánh an toàn/effectiveness giữa liều tiêu chuẩn và liều tùy chỉnh theo S-values cá nhân.
Hệ số RBE và liều hiệu quả: công thức tính liều nặng tính RBE (như MIRD-RBE) cần hiệu chỉnh dựa trên thử nghiệm sinh học. Cần đo RBE thực tế in vivo của các đồng vị α mới trên các mô đặc hiệu (ví dụ RBE của 225Ac với u PSMA so với 177Lu). Đề xuất đo RBE trên mô nuôi ba chiều hoặc mô hình động vật so sánh α và β cùng liều hấp thụ.
Sản xuất đồng vị: mặc dù nhiều dự án quy mô lớn đang triển khai, nhu cầu về 225Ac, 211At, 161Tb… vẫn vượt cung. Cần nghiên cứu thêm quy trình tách chiết hiệu quả hơn: ví dụ xúc tác proton-máy xúc tác, neutron nặng (multipliers) để tăng yield. Song song, phát triển trung tâm sản xuất khu vực (regional facilities) để rút ngắn vận chuyển. Một đề xuất: làm rõ sử dụng các linh kiện tái sử dụng (227Th generator để sinh 223Ra tại bệnh viện, hay 68Ge/68Ga model cho 225Ac) nhằm cải thiện an ninh chuỗi cung ứng.
Thiết kế thử nghiệm lâm sàng mới: ưu tiên thử nghiệm so sánh (randomized) các radionuclide mới kết hợp với tương tác thuốc khác (ví dụ: 225Ac-PSMA cộng liệu pháp ức chế PARP đối với ung thư tiền liệt tuyến PSMA+, hoặc 211At-kháng thể định hướng + hóa trị). Cần đo lường các chỉ số kép: dược động học (hình ảnh phân bố từng liều), hiệu quả sinh học (hình ảnh sau điều trị hoặc mẫu sinh thiết), và đánh giá độc tính theo từng giai đoạn.
Chỉ số phụ trợ và biomarker: nghiên cứu để tìm các biomarker tiên đoán đáp ứng TRT (hàm lượng PSMA, PSAdoubling time, gene expression) và quan hệ dose-response. Đặc biệt, cần giám sát độc tính cấp, đề xuất các dấu ấn (biomarker) của tổn thương gan/thận do TRT (như phân tử viêm, protein tế bào ống thận trong nước tiểu) cho phép can thiệp kịp thời.
Để hạn chế khoảng trống thụ hưởng liệu pháp này, cần đầu tư đào tạo chuyên ngành (medical physics, radiochemistry) và phổ biến hướng dẫn lâm sàng (của SNMMI, EANM). Nhiều bác sĩ lâm sàng vẫn chưa quen với xạ trị liều thấp (mGy) nhưng kéo dài, nên phải đồng bộ các khuyến nghị liều tối ưu.
Bảng so sánh các đồng vị phóng xạ tiêu biểu
| Đồng vị | Chu kỳ bán rã (T½) | Phóng xạ phát | Năng lượng phát (E) | Khoảng xuyên (range) | Phương pháp sản xuất | Ứng dụng lâm sàng chính |
| 225Ac | ~9.9 ngày | α (đa phát) | ~5–8 MeV (tổng chuỗi ~25 MeV) | ~50–100 µm | Th-229 (generator); p+232Th (accelerator); Giải phóng từ U-233 (TerraPower) | Nghiên cứu RPT (PSMA, DOTATOC…) |
| 211At | ~7.2 giờ | α (100%) | ~6 MeV (α chủ yếu) | ~50–80 µm | Cyclotron: 209Bi(α,2n)211At | Nghiên cứu RPT (tiểu thể, khối đặc) |
| 223Ra | ~11.4 ngày | α (100%) | 5.7 MeV (trung bình) | ~80 µm | Máy tạo: sinh từ 227Th hoặc phân rã tự nhiên (phản ứng Neutron) | Xương (ung thư tiền liệt tuyến di căn) |
| 212Pb | ~10.6 giờ | β- (64%); α từ 212Po | β- 0.6 MeV; α 6.05 MeV | β- ~5 mm; α ~50 µm | Generator từ 228Th (232Th) | R&D (α-peptide, α-IgG) |
| 177Lu | ~6.65 ngày | β- (100%); γ 113,208 keV | β- Emax 0.497 MeV (R~2 mm) | β- ~2 mm | Reactor: 176Lu(n,γ)177Lu trên Lu giàu; pp: 176Yb(p,n)177Lu | NET (Lutathera); ung thư tiền liệt tuyến (PSMA) |
| 161Tb | ~6.9 ngày | β-; IC, Auger; γ 48-75 keV | β- Emax ~0.6 MeV (R~1 mm); nhiều electron <40 keV | β- ~1 mm | Reactor: 60Gd(n,γ)161Gd→161Tb | Theranostics (imaging + therapy thử nghiệm) |
| 90Y | ~64 giờ | β- (100%) | Emax 2.28 MeV (R~11 mm) | ~11 mm | 90Sr/90Y generator | Y khoa (xạ trị bạch cầu [Zevalin], đau xương) |
| 131I | ~8.02 ngày | β-; γ 364 keV | β- Emax 0.61 MeV (R~2 mm) | ~2 mm | Reactor: 130Te(n,γ)131Te→131I | Tuyến giáp (ung thư tuyến giáp, cường giáp) |
Các đồng vị tiên tiến phải qua nhiều giai đoạn trước khi ứng dụng rộng. Dưới đây là một sơ đồ roadmap giai đoạn và thời gian dự kiến cho một liệu pháp phóng xạ mới:
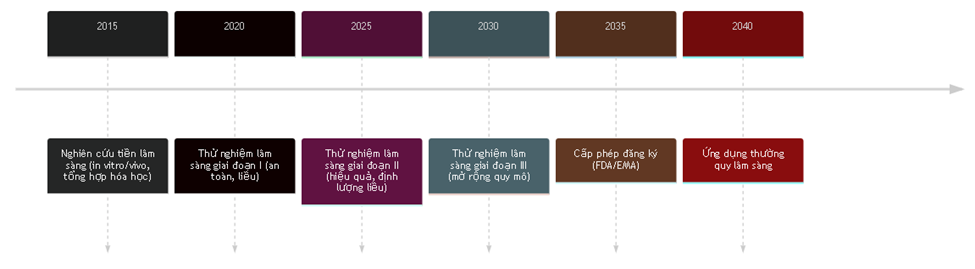
Trong giai đoạn tiền lâm sàng, tập trung xây dựng mẫu liên hợp (đồng vị–chelator–vectơ), khảo sát tính ổn định, phân bố thụ thể và độc tính ở động vật (thường chuột và thỏ). Sau đó, giai đoạn I đánh giá dược động học và an toàn ở người tình nguyện khỏe mạnh hoặc bệnh nhân giai đoạn cuối. Giai đoạn II (có so sánh nhóm chứng) xác định hiệu quả ước lượng ban đầu (PFS/PSA). Giai đoạn III là thử nghiệm đa trung tâm quy mô lớn chứng minh lợi ích sống còn, sau khi đó nhà quản lý cấp phép. Quá trình này thường kéo dài ~10–15 năm từ ý tưởng đến phê duyệt. Tuy nhiên, do nhu cầu cấp bách và kiến thức sẵn có, nhiều bước có thể chạy song song (ví dụ song song tăng công suất sản xuất với phát triển lâm sàng).
Từ khóa: thuốc phóng xạ;
– CMD –