Trong kho chứa nhiên liệu hạt nhân đã qua sử dụng, hợp chất studtite (UO2)O2(H2O)4 hình thành trên bề mặt nhiên liệu khi tiếp xúc với nước khi có một số điều kiện nhất định. Studtite có độ hòa tan rất thấp và do đó có thể làm giảm khả năng phản ứng của nhiên liệu hạt nhân đã qua sử dụng đối với chất oxy hóa phân hủy phóng xạ. Điều này sẽ ức chế khả năng hòa tan nhiên liệu và cũng ức chế sự phát tán của các chất phóng xạ. Điều quan trọng là phải hiểu rõ tính ổn định của studtite trong các điều kiện môi trường. Nghiên cứu mới đây của các nhà khoa học hướng tới động học quá trình hòa tan studtite trong hỗn dịch nước không chứa HCO3– thêm vào và có 10 mM HCO3–, dung dịch chứa 0,2 mM H2O2. Độ hòa tan của studtite trong hỗn dịch đó là rất thấp. Ngoài ra, sự hòa tan studtite do bức xạ γ gây ra trong các dung dịch thiếu HCO3– và trong 10 mM HCO3– cũng đã được làm rõ. Tốc độ hòa tan được phát hiện là cực kỳ cao trong HCO3– với sự chiếu xạ γ.

Ở một số quốc gia, các kho chứa sâu dưới lòng đất được coi là giải pháp thay thế an toàn nhất cho việc xử lý lâu dài nhiên liệu hạt nhân đã qua sử dụng. Do khoảng thời gian cực kỳ dài mà tính toàn vẹn của các lớp che chắn được sử dụng trong kho phải được giữ nguyên để đảm bảo an toàn cho kho, nên việc nghiên cứu mọi quy trình có thể ảnh hưởng đến các lớp che chắn là vô cùng quan trọng. Để có thể đánh giá hậu quả của việc nhiều lớp che chắn bị hỏng, điều cần thiết là phải nghiên cứu động học và cơ chế của các quy trình có thể xảy ra khi nhiên liệu hạt nhân đã qua sử dụng tiếp xúc với nước ngầm, đặc biệt là các quy trình ảnh hưởng đến sự phát tán các chất phóng xạ từ nhiên liệu hạt nhân đã qua sử dụng. Các loại nhiên liệu hạt nhân thương mại phổ biến nhất dựa trên UO2 và vì tỷ lệ phân hạch của urani trong nhiên liệu khá thấp nên UO2 cũng là thành phần chính của nhiên liệu hạt nhân đã qua sử dụng. Ngoài UO2, nhiên liệu hạt nhân đã qua sử dụng còn chứa khoảng 5% sản phẩm phân hạch phóng xạ và các actinide nặng hơn.
Người ta cho rằng các chất phóng xạ độc hại được giải phóng vào nước ngầm, chủ yếu là khi hòa tan UO2. Tại các địa điểm kho chứa tiềm năng, nước ngầm thường bị khử và trong những điều kiện này, độ hòa tan của UO2 rất thấp. Tuy nhiên, bức xạ ion hóa phát ra từ nhiên liệu hạt nhân đã qua sử dụng sẽ được nước ngầm hấp thụ, dẫn đến sự phân ly phóng xạ của nước. Sự phân ly phóng xạ của nước tạo ra chất oxy hóa (HO•, H2O2 và HO2•) cũng như chất khử (eaq–, H• và H2). Vì lý do động học, các phản ứng bề mặt, ít nhất là ban đầu, sẽ bị chi phối bởi các chất oxy hóa làm tăng đáng kể độ hòa tan của ma trận UO2 (U(VI) hòa tan nhiều bậc độ lớn hơn U(IV)). Quá trình hòa tan được đẩy nhanh hơn nữa bởi thành phần nước ngầm phổ biến HCO3– vì UO22+ dễ dàng tạo thành các phức hợp cacbonat có độ hòa tan cao. Trong số các chất oxy hóa phân ly phóng xạ, H2O2 đã được chứng minh là chi phối quá trình hòa tan oxy hóa của UO2 trong điều kiện kho chứa.
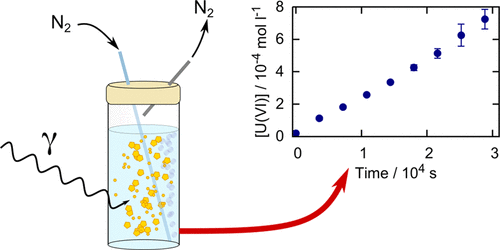
H2O2 có thể phản ứng với UO22+ để tạo thành studtite, (UO2)O2(H2O)4, hoặc sản phẩm tách nước của nó là metastudtite, (UO2)O2(H2O)2. Hai pha này có độ hòa tan rất thấp và theo quan điểm nhiệt động lực học, studtite sẽ được hình thành khi oxy hóa UO2 bởi H2O2 ngay cả khi có mặt HCO3–dù điều này, theo hiểu biết hiện nay, chưa bao giờ được báo cáo. Tuy nhiên, trong các hệ thống thiếu HCO3–, studtite hoặc metastudtite được phát hiện kết tủa trên bề mặt UO2 và do đó làm giảm khả năng phản ứng của nó. Khi có mặt H2O2, sự hình thành studtite thuận lợi về mặt nhiệt động lực học hơn so với sự hình thành uranyl oxide hydrat và uranyl silicat. Sự tồn tại của studtite và metastudtite trên bề mặt nhiên liệu hạt nhân đã qua sử dụng thương mại đã được Hanson xác nhận sau khi ngâm các mảnh nhiên liệu trong nước khử ion trong hơn 2 năm ở nhiệt độ phòng. Trong các thí nghiệm của họ, nhiễu xạ tia X (XRD) cho thấy studtite và UO2 là các pha chính trong tất cả các mẫu, trong khi metastudtite chỉ được xác định trong các chất rắn nổi trên giao diện không khí-nước của mẫu. Nguồn H2O2 trong các thí nghiệm này là quá trình phân hủy phóng xạ nước. Hơn nữa, các thí nghiệm hòa tan oxy hóa trên UO2 được Clarens và cộng sự thực hiện và đã chỉ ra rằng ở nồng độ H2O2 thấp (5 × 10–3 mM), nồng độ urani tăng theo thời gian. Tuy nhiên, ở nồng độ H2O2 cao hơn (0,5 mM), nồng độ urani ở trạng thái ổn định và hình thành kết tủa màu vàng. Kết tủa sau được xác định là studtite. Do đó, sự hình thành studtite trên bề mặt nhiên liệu hạt nhân đã qua sử dụng có thể ảnh hưởng đến tính ổn định lâu dài của nhiên liệu hạt nhân đã qua sử dụng trong kho chứa sau khi nước ngầm xâm nhập.
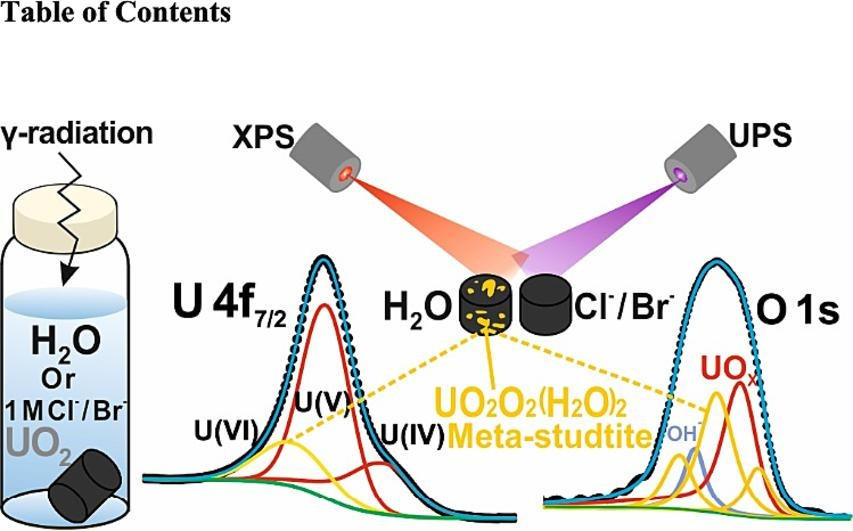
Các viên UO2 tiếp xúc với bức xạ γ – đặc trưng bằng cách sử dụng Phổ quang điện tử tia X (XPS) và Phổ quang điện tử cực tím (UPS) để nghiên cứu trạng thái oxy hóa của U và khả năng thay đổi bề mặt
Điều thú vị là mặc dù độ hòa tan của studtite nhìn chung khá thấp, nhưng ngày càng có nhiều bằng chứng cho thấy sự hình thành nanocluster có thể hòa tan studtite hiệu quả trong một số điều kiện nhất định. Các nanocluster uranyl peroxide cũng có thể được hình thành từ các hợp chất urani rắn khác ngoài studtite. Ngoài ra, uranyl đã được chứng minh là tạo thành nhiều phức chất khác nhau với hydro peroxide và cacbonat. Sự hiện diện của cacbonat ngăn cản sự hình thành các cụm lớn hơn. Động lực học hòa tan của studtite trong dung dịch HCO3– thiếu và HCO3– 10 mM đã được nghiên cứu thực nghiệm để đánh giá tác động của HCO3–.
Kết quả đánh giá cho thấy độ hòa tan của studtite trong hỗn dịch không có HCO3– bổ sung là rất thấp. Trong hỗn dịch chứa 10 mM HCO3–, độ hòa tan quan sát được cao hơn đáng kể. Điều này là do sự hình thành các phức hợp uranyl–carbonate và uranyl–peroxo–carbonate. Với sự hiện diện của 0,2 mM H2O2 và 10 mM HCO3–, độ hòa tan cao hơn dự kiến nếu chỉ tính đến phức hợp carbonate nhưng hợp lý nếu cũng tính đến các phức hợp uranyl–peroxo–carbonate. Điều thú vị là các thí nghiệm cho thấy H2O2 bị phân hủy xúc tác khi có uranyl–carbonate. Các thí nghiệm cũng cho thấy H2O2 không biểu hiện bất kỳ phản ứng đáng kể nào đối với bề mặt studtite. Khi tiếp xúc với bức xạ γ, studtite trong hỗn dịch nước chứa 10 mM HCO3– hòa tan nhanh chóng. Sự hòa tan rất nhanh này là do sự kết hợp giữa quá trình phân hủy phóng xạ của H2O2 và sự hình thành các phức hợp uranyl–peroxo–carbonate, giữ nồng độ H2O2 tự do ở mức rất thấp và do đó thúc đẩy quá trình hòa tan.
Từ khóa: phóng xạ; nhiêu liệu hạt nhân;
– CMD –






