Ngày nay, các đồng vị phóng xạ đã trở thành nền tảng của y học kể từ khi chúng được phát hiện. Từ các ứng dụng nội mô ban đầu của radium và 137Cs đến ứng dụng hiện đại của các thiết bị nạp sau 192Ir và 125I trong xạ trị áp sát, các đồng vị phóng xạ vẫn là công cụ điều trị cho bệnh ung thư tuyến tiền liệt, phụ khoa và vùng đầu cổ. Tuy nhiên, sự phát xạ liên tục của các nguồn phóng xạ và đặc biệt là các nguồn phóng xạ hoạt độ cao cũng gây ra nhiều vấn đề trong lưu giữ, sử dụng, quy định an ninh. Do đó, các cơ quan quản lý quốc tế khuyến cáo giảm thiểu sự phụ thuộc vào các nguồn có hoạt độ cao khi có thể. Những tiến bộ trong các phương thức xạ trị hướng dẫn bằng hình ảnh đã tạo ra các nền tảng lâm sàng hoàn thiện có khả năng cung cấp liều cao mà vẫn bảo tồn được các mô bình thường khỏi phóng xạ. Các công nghệ mới nổi hiện nay đang hướng tới cách tiếp cận đó và giải quyết nhiều vấn đề về bức xạ liều cao, bao gồm năm phương thức: (1) liệu pháp nhiệt nội mô bằng laser; (2) liệu pháp xạ trị trong phẫu thuật, sử dụng tia X hoặc electron kV thấp; (3) máy gia tốc tuyến tính hướng dẫn bằng MRI (MR-LINAC); (4) liệu pháp chiếu xạ ngoài “FLASH” với tốc độ liều cực cao; (5) liệu pháp hạt sử dụng proton và ion nặng. Những công nghệ này hứa hẹn các lựa chọn điều trị không phóng xạ, có độ chính xác cao, tận dụng các cơ chế sinh học phóng xạ đa dạng để định nghĩa lại tỷ lệ điều trị trong thực hành lâm sàng.
Các đồng vị phóng xạ đã trở thành nền tảng của y học bức xạ kể từ khi hiện tượng phóng xạ được Henri Becquerel phát hiện vào năm 1896 và sau đó là tách chiết radium bởi Marie Curie và Pierre Curie. Những ứng dụng ban đầu của radium trong xạ trị áp sát trong khoang (intracavitary) và xạ trị áp sát trong mô (interstitial) hay sử dụng cesium-137 (¹³⁷Cs) và iridium-192 (¹⁹²Ir), đã chứng minh rằng các đồng vị phóng xạ có thể được sử dụng để đưa liều bức xạ “từ bên trong ra ngoài”, từ đó đặt nền móng cho xạ trị áp sát hiện đại (brachytherapy). Ngày nay, các thiết bị nạp nguồn sau suất liều cao (HDR) sử dụng ¹⁹²Ir và các hạt giống phóng xạ suất liều thấp (LDR) ¹²⁵I đã trở thành phương pháp điều trị tiêu chuẩn cho nhiều loại ung thư như ung thư tuyến tiền liệt, ung thư phụ khoa, và ung thư vùng đầu – cổ.
Tuy nhiên, chính những đặc điểm khiến nguồn phóng xạ kín trở nên hấp dẫn, đặc biệt là sự phát xạ liên tục và hoạt độ riêng cao, lại đồng thời tạo ra những rào cản đáng kể trong môi trường y tế. Ví dụ, các cơ sở y tế sử dụng đồng vị phóng xạ phải xây dựng các hầm che chắn chuyên dụng và thực hiện kiểm kê, quản lý nguồn nghiêm ngặt nhằm giảm thiểu nguy cơ các nguồn có hoạt độ cao bị sử dụng cho mục đích xấu. Bên cạnh đó, chuỗi cung ứng toàn cầu đối với các đồng vị được sản xuất từ lò phản ứng hạt nhân khá mong manh; việc tạm dừng hoạt động của các lò phản ứng hoặc những gián đoạn địa chính trị thường xuyên dẫn đến tình trạng thiếu hụt ¹⁹²Ir. Vì vậy, các cơ quan quản lý trong nước và các tổ chức quốc tế đã đề ra mục tiêu dài hạn là thay thế, hoặc ít nhất là giảm thiểu, sự phụ thuộc vào các nguồn phóng xạ kín có hoạt độ cao, khi điều đó là khả thi.
Song song với đó, các thế hệ công nghệ mới được dẫn hướng bằng hình ảnh và tập trung năng lượng đã phát triển đến mức có thể bổ sung hoặc thậm chí thay thế các liệu pháp dựa trên đồng vị phóng xạ, trong khi vẫn duy trì đặc tính gradient liều rất dốc và bảo vệ mô lành. Năm phương pháp hiện đang bước vào thực hành lâm sàng thường quy hoặc các thử nghiệm then chốt:
- Liệu pháp nhiệt kẽ bằng laser (Laser Interstitial Thermal Therapy – LITT): hệ thống laser định vị lập thể (stereotactic) được dẫn hướng bằng đo nhiệt MR (MR thermography), có khả năng đốt hủy khối u với độ chính xác dưới milimet.
- Xạ trị trong mổ (Intra-Operative Radiation Therapy – IORT): sử dụng tia X năng lượng thấp (kV) hoặc chùm electron được chiếu ngay sau khi khối u được cắt bỏ trong phẫu thuật.
- Máy gia tốc tuyến tính dẫn hướng bằng MRI (MRI-guided Linear Accelerator – MR-LINAC): sự tích hợp MRI ≥1,5 T với máy gia tốc tuyến tính 6–7 MV, cho phép theo dõi mô mềm theo thời gian thực và lập kế hoạch xạ trị thích ứng ngay trên bàn điều trị, từ đó giảm biên mục tiêu và giảm liều cho các cơ quan nguy cấp (organs at risk).
- Xạ trị chùm ngoài suất liều siêu cao (FLASH): cung cấp liều >40 Gy/s trong khoảng thời gian micro-giây, đã cho thấy khả năng bảo vệ mô lành trong các nghiên cứu tiền lâm sàng.
- Liệu pháp hạt (particle therapy – proton và ion nặng): sử dụng các hạt mang điện có khối lượng lớn, cho phép phân bố liều chính xác tại đỉnh Bragg (Bragg peak).
Các nền tảng công nghệ này nhằm truyền năng lượng cao vào mô đích mà không để lại dấu vết phóng xạ. Đồng thời, chúng cũng cho phép khai thác nhiều cơ chế sinh học bức xạ khác nhau, từ cơ chế tiêu diệt tế bào ít phụ thuộc vào oxy của ion carbon đến hiệu ứng suất liều siêu nhanh của FLASH, những yếu tố có thể định nghĩa lại tỷ lệ hiệu quả điều trị (therapeutic ratio) trong thực hành lâm sàng.
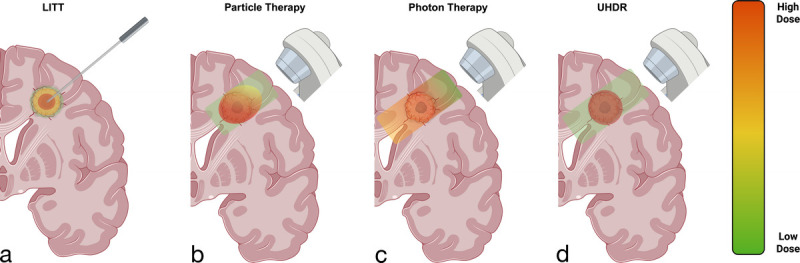
Liệu pháp nhiệt kẽ bằng laser (Laser Interstitial Thermal Therapy – LITT) là kỹ thuật xâm lấn tối thiểu sử dụng tăng thân nhiệt có kiểm soát để phá hủy mô khối u. Quy trình này bao gồm việc đưa một đầu dò sợi quang mảnh vào trong khối u dưới hướng dẫn hình ảnh thời gian thực, thường sử dụng MRI hoặc CT. Sau khi đầu dò được đặt đúng vị trí, chụp MRI sẽ xác nhận vị trí trước khi tia laser được kích hoạt thông qua một bảng điều khiển bên ngoài phòng mổ. Laser truyền năng lượng nhiệt, làm nóng mô xung quanh và gây ra hoại tử đông tụ (coagulative necrosis). Đo nhiệt bằng MRI (MRI thermometry) liên tục theo dõi nhiệt độ mô thông qua kỹ thuật dịch chuyển tần số cộng hưởng proton (Proton Resonance Frequency Shift – PRFS), tạo ra bản đồ nhiệt theo thời gian thực nhằm bảo đảm liều nhiệt chính xác và tránh tổn thương các cấu trúc quan trọng.
Kỹ thuật này ban đầu được phê duyệt cho các ứng dụng phẫu thuật thần kinh tại Hoa Kỳ, sau đó đã được U.S. Food and Drug Administration phê duyệt để điều trị u não, động kinh, hoại tử do bức xạ và các tổn thương di căn. Ngoài não, LITT còn được sử dụng để điều trị khối u gan, tuyến tiền liệt và cột sống, cung cấp một lựa chọn xâm lấn tối thiểu thay thế cho phẫu thuật hoặc xạ trị truyền thống. Khi xem xét LITT như một phương án thay thế cho xạ trị dựa trên đồng vị phóng xạ, một trong những ưu điểm quan trọng nhất nằm ở cơ chế tác động. Khác với xạ trị sử dụng đồng vị phóng xạ, dựa trên sự phát xạ dần dần của bức xạ ion hóa từ các nguồn phóng xạ cấy ghép hoặc đưa vào cơ thể, LITT tạo ra hiệu ứng phá hủy mô tức thời và khu trú bằng nhiệt do laser sinh ra. Điều này loại bỏ sự phơi nhiễm bức xạ kéo dài và cho phép kiểm soát các thông số điều trị theo thời gian thực.
LITT cũng mang lại độ chính xác cao trong phân bố liều nhiệt. MRI thermometry cung cấp phản hồi theo thời gian thực về phân bố nhiệt độ, cho phép điều chỉnh ngay lập tức để đảm bảo tiêu diệt khối u hiệu quả trong khi bảo tồn mô lành xung quanh. Ngược lại, xạ trị dựa trên đồng vị phóng xạ phụ thuộc vào phân bố liều bức xạ được tính toán trước, và không thể điều chỉnh chủ động sau khi đã đưa nguồn vào cơ thể, điều này có thể dẫn đến sự biến thiên liều. Từ góc độ an toàn và quản lý, LITT có những lợi thế nhất định, vì không sử dụng vật liệu phóng xạ, loại bỏ các vấn đề liên quan đến phơi nhiễm bức xạ, sự phân rã đồng vị và nguy cơ ô nhiễm môi trường. Bệnh nhân điều trị bằng xạ trị đồng vị phóng xạ đôi khi phải tuân thủ các biện pháp an toàn bức xạ để bảo vệ người chăm sóc và người thân, đặc biệt trong trường hợp dược chất phóng xạ dùng đường toàn thân. Ngoài ra, LITT đã được FDA phê duyệt cho điều trị u não, động kinh và các tổn thương di căn, trong khi các liệu pháp mới dựa trên đồng vị phóng xạ có thể phải đối mặt với những rào cản quản lý nghiêm ngặt hơn do các quy định về an toàn bức xạ.
Quy trình lâm sàng và khả năng triển khai của LITT cũng mang lại lợi ích thực tế. Những bệnh viện không có khoa xạ trị chuyên biệt có thể dễ dàng áp dụng LITT hơn do ít ràng buộc về quy định và an toàn bức xạ. LITT còn có tiềm năng trong các liệu pháp kết hợp. Tương tự như các chất tăng nhạy bức xạ dựa trên đồng vị, tăng thân nhiệt do LITT có thể tăng cường hiệu quả của xạ trị bằng cách làm tăng độ nhạy của khối u đối với tổn thương do bức xạ ion hóa. LITT cũng được biết đến là một tác nhân mạnh làm gián đoạn hàng rào máu–não (Blood–Brain Barrier – BBB), nhờ đó có thể tận dụng các thuốc hóa trị toàn thân trong điều trị u não vốn trước đây khó vượt qua BBB.
Tuy nhiên, so với các liệu pháp dựa trên đồng vị phóng xạ, LITT có hai hạn chế chính. Thứ nhất, vùng và phạm vi phá hủy mô của LITT bị giới hạn bởi đặc tính “tản nhiệt” (heatsink) của mô, điều này có thể giới hạn hiệu quả đối với các khối u lớn. Trong điều trị u não, vùng tăng thân nhiệt phá hủy thường chỉ đạt đường kính khoảng 2–3 cm. Để khắc phục hạn chế này, các bác sĩ có thể sử dụng nhiều sợi quang đồng thời, kỹ thuật rút đầu dò từng bước (fiber pullback), hoặc sợi laser có đầu khuếch tán kéo dài. Hạn chế thứ hai là LITT yêu cầu MRI trong phòng mổ để theo dõi nhiệt độ theo thời gian thực. Mặc dù khả năng quan sát trực tiếp quá trình phá hủy mô và điều chỉnh điều trị ngay trong lúc thực hiện mang lại độ chính xác và tính linh hoạt cao, nhưng hệ thống MRI 3 T trong phòng mổ hiện nay chủ yếu chỉ có tại các trung tâm phẫu thuật thần kinh lớn ở Hoa Kỳ. Tuy nhiên, các chuỗi xung MRI thermography sử dụng trong LITT có thể thực hiện trên hầu hết các máy MRI chẩn đoán 3 T hiện đại, vốn phổ biến hơn, mở ra khả năng triển khai rộng rãi công nghệ này trong tương lai.
Xạ trị trong mổ (Intraoperative Radiotherapy – IORT) nhằm đưa bức xạ trực tiếp tới khối u cần điều trị hoặc tới giường khối u xung quanh, trong bối cảnh phẫu thuật hoặc can thiệp xâm lấn. Các phương pháp IORT hiện nay chủ yếu truyền bức xạ thông qua chùm tia chiếu trực diện (en-face beam) hoặc thông qua các đầu áp (applicator), với nhiều hình dạng đầu áp khác nhau. So với xạ trị chùm ngoài truyền thống, IORT có một số lợi ích đáng kể, bao gồm khả năng chiếu xạ trực tiếp vào thể tích khối u đã được cắt bỏ ngay trong quá trình phẫu thuật, từ đó giảm nhu cầu bệnh nhân phải đến cơ sở xạ trị nhiều lần. Các thiết bị IORT cũng tận dụng việc sử dụng tia X ở mức năng lượng thấp (kV) so với các hệ thống xạ trị chùm ngoài truyền thống. Điều này làm tăng tốc độ suy giảm liều theo khoảng cách (dose fall-off) và tăng khả năng bảo vệ các cơ quan hoặc vùng mô không phải mục tiêu. Khả năng cung cấp liều cao cho giường khối u ngay tại thời điểm cắt bỏ khối u đã khiến các phương pháp IORT có hiệu quả tiêu diệt khối u rất mạnh.
Đối với IORT không sử dụng chùm tia en-face, nhiều loại đầu áp đã được đưa ra thị trường, bao gồm:
- Đầu áp trường phẳng truyền thống (flat-field applicator) – phù hợp cho xạ trị chùm ngoài.
- Đầu áp dạng kim (needle applicator).
- Đầu áp dạng cầu (spherical applicator).
Đầu áp trường phẳng được sử dụng để truyền bức xạ trực diện vào thể tích khối u đã được cắt bỏ. Trong khi đó, đầu áp dạng kim và dạng cầu cho phép bác sĩ đưa bức xạ trực tiếp khi đầu áp tiếp xúc với vùng giường khối u.
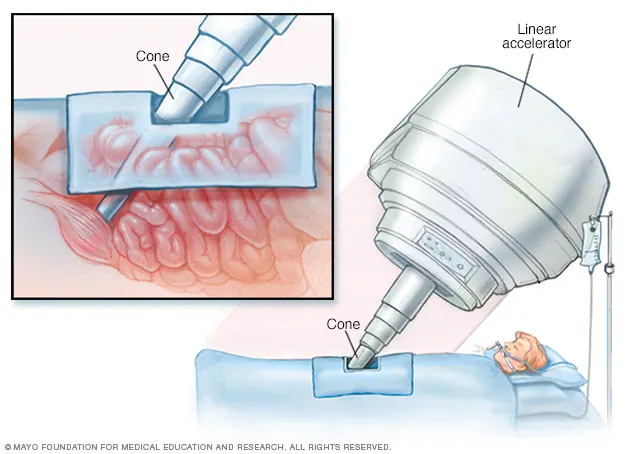
Đầu áp dạng kim đặc biệt hữu ích trong điều trị ung thư di căn cột sống, vì nó có thể được đưa trực tiếp vào vùng cần điều trị, cho phép chiếu xạ các vùng xung quanh ngay lập tức với sự suy giảm liều nhanh theo chiều sâu. Ngược lại, đầu áp dạng cầu được sử dụng trong IORT điều trị ung thư vú và trong phẫu thuật thần kinh để điều trị di căn não.
Mặc dù IORT cho thấy nhiều triển vọng trong việc mở ra một kỷ nguyên mới của xạ trị được thực hiện ngay trong quá trình phẫu thuật, phương pháp này vẫn có những hạn chế quan trọng so với xạ trị áp sát bằng đồng vị phóng xạ hoặc xạ trị chùm ngoài truyền thống. Các thiết bị IORT hiện nay sử dụng tia X năng lượng thấp (kilovoltage), nam châm điều khiển quỹ đạo chùm tia, và các đầu áp đặt trong khoang phẫu thuật để truyền bức xạ phù hợp với hình dạng khoang phẫu thuật và tạo ra sự suy giảm liều nhanh từ bề mặt mô. Điều này đặt ra những thách thức đặc biệt đối với các nhà vật lý y học và bác sĩ xạ trị, đặc biệt trong hai khía cạnh: đảm bảo chất lượng (Quality Assurance – QA) về tính đồng nhất của chùm tia; lập kế hoạch điều trị chính xác, có tính đến các phức tạp về liều lượng trong khoang phẫu thuật.
Xạ trị dẫn hướng bằng MRI (MRgRT) đại diện cho sự hợp nhất giữa hai nhánh chẩn đoán và điều trị của chuyên ngành xạ trị ung thư. Chụp cộng hưởng từ (MRI) khai thác sự tương tác giữa từ hóa hạt nhân và spin hạt nhân của một số đồng vị với từ trường và môi trường cục bộ của chúng, từ đó cung cấp hình ảnh ba chiều rõ ràng về giải phẫu và sinh lý của bệnh nhân. Các đồng vị hạt nhân này, vốn có sẵn với số lượng lớn trong cơ thể hoặc được đưa vào từ nguồn bên ngoài, có thể được khảo sát theo những cách đặc biệt để tạo ra độ tương phản mô vượt trội mà không cần sử dụng bức xạ ion hóa. Bằng cách tận dụng độ tương phản của MRI cùng với khả năng phân phối liều chính xác của các máy gia tốc tuyến tính hiện đại, các nhóm lâm sàng có thể sử dụng các kỹ thuật gating chuyển động cải tiến và hình ảnh chức năng để quản lý liều bức xạ được cung cấp cho bệnh nhân.
Sự kết hợp đỉnh cao của hai công nghệ này là hệ thống MR-LINAC, có khả năng theo dõi ranh giới khối u theo thời gian thực cũng như quản lý chuyển động giữa các phân liều và trong từng phân liều, cho phép lập kế hoạch điều trị thích ứng và kiểm soát tốt hơn liều bức xạ ngoài mục tiêu. Hiện mới chỉ có hai nhà cung cấp lớn các hệ thống MR-LINAC: Elekta với hệ thống Unity (Stockholm, Thụy Điển); ViewRay với hệ thống MRIdian (Bedford, Ohio, Hoa Kỳ). Hai hệ thống này khác biệt đáng kể về thiết kế và cường độ từ trường (1,5 T đối với Unity; 0,35 T đối với MRIdian), trong đó mỗi hệ thống đánh đổi giữa chất lượng hình ảnh và khả năng phân bố liều bức xạ tối ưu. Từ trường mạnh hơn giúp cải thiện chất lượng hình ảnh, nhưng lại làm tăng liều tán xạ electron tại ranh giới mô–không khí do hiệu ứng lực Lorentz. Hiện tượng này có thể được bù trừ bằng các cấu hình chùm tia phụ thuộc hướng.
Một vấn đề khác là các hệ thống MR-LINAC không cung cấp dữ liệu mật độ điện tử, vốn cần thiết để tính toán trực tiếp sự lắng đọng liều bức xạ. Vì vậy, mạng nơ-ron tích chập sâu (deep convolutional neural networks) đang được nghiên cứu để tạo ra ảnh CT tổng hợp (synthetic CT – sCT) từ dữ liệu MRI. Trong thực hành lâm sàng, MRgRT đặc biệt hữu ích trong điều trị:
- Các khối u không thể phẫu thuật,
- Các khối u di căn ít ổ (oligometastatic),
- Các khối u chịu ảnh hưởng bởi chuyển động hô hấp hoặc tim mạch.
Phương pháp này đã được ứng dụng thành công trong điều trị ung thư vú, hạch bạch huyết, thận, gan và trực tràng. Đặc biệt, ung thư biểu mô tuyến ống tụy (Pancreatic Ductal Adenocarcinoma – PDAC) có thể cải thiện kết quả điều trị khi MRgRT được áp dụng xen kẽ giữa các chu kỳ hóa trị.

Về mặt khái niệm, MRgRT có thể được xem như một phương pháp tương tự với xạ trị dựa trên đồng vị phóng xạ: cả hai cách tiếp cận đều kết hợp giữa hình ảnh và phân phối liều điều trị, sao cho tín hiệu vật lý dùng để quan sát khối u cũng đồng thời hướng dẫn liều điều trị. Trong khi xạ trị đồng vị phóng xạ kết hợp phân bố liều nội tại của các nguồn phóng xạ cấy ghép với định vị giải phẫu, thì MR-LINAC kết hợp hình ảnh MRI có độ tương phản cao với chùm photon được định hướng chính xác, đạt được sự đồng đăng ký (co-registration) theo thời gian thực và cho phép điều chỉnh kế hoạch điều trị ngay trên bàn xạ trị. Tuy nhiên, hai hạn chế thực tế khiến MRgRT không thể trở thành giải pháp thay thế hoàn toàn cho xạ trị đồng vị phóng xạ.
Thứ nhất là hạ tầng kỹ thuật. MRgRT yêu cầu phòng điều trị MR-LINAC chuyên dụng với hệ thống che chắn, chùm tia được bảo vệ khỏi ảnh hưởng của từ trường, quy trình đảm bảo chất lượng nghiêm ngặt, và đội ngũ đa ngành được đào tạo cả về vật lý MRI lẫn xạ trị ung thư. Các yêu cầu về đầu tư và nhân lực này khiến công nghệ chỉ được triển khai tại một số trung tâm y khoa tuyến cao, trong khi nhiều liệu pháp đồng vị phóng xạ có thể thực hiện trong phòng che chắn tiêu chuẩn hoặc thậm chí ở cơ sở ngoại trú.
Hạn chế thứ hai liên quan đến phạm vi tác động sinh học bức xạ. Các đồng vị phóng xạ phát bức xạ từ bên trong khối u, tạo ra phân bố liều “từ trong ra ngoài” đồng đều. Ngược lại, MRgRT vẫn dựa vào chùm photon từ bên ngoài, mà gradient liều theo chiều sâu, sự không đồng nhất của mô và ảnh hưởng của chuyển động có thể dẫn đến tăng liều ở mô lành nằm trên đường đi của chùm tia. Do đó, mặc dù MRgRT cung cấp khả năng dẫn hướng giải phẫu vượt trội cho các tổn thương khu trú, phương pháp này chưa thể tái tạo được các ưu thế về phân bố liều toàn bộ của các liệu pháp dựa trên đồng vị phóng xạ, và vẫn bị giới hạn bởi yêu cầu về hạ tầng và thiết bị chuyên biệt.
Xạ trị suất liều siêu cao (Ultra-High Dose Rate – UHDR), thường là >40 Gy/s, đã được chứng minh là tạo ra “hiệu ứng FLASH”, trong đó mô lành được bảo vệ tốt hơn khi khả năng kiểm soát khối u vẫn tương đương với xạ trị ở suất liều thông thường (Conventional Dose Rate – CDR). Các nghiên cứu tiền lâm sàng cho thấy hiệu ứng FLASH có thể được trung gian bởi:
- Sự suy giảm nhanh nồng độ oxy;
- Những thay đổi trong sinh học của các loại oxy phản ứng (Reactive Oxygen Species – ROS);
- Giảm phản ứng viêm trong mô lành.
Hiện nay, nhiều thử nghiệm lâm sàng đang được tiến hành ở châu Âu và Hoa Kỳ nhằm đánh giá xạ trị UHDR, nhưng việc triển khai rộng rãi công nghệ này trong lâm sàng vẫn gặp nhiều thách thức kỹ thuật và sinh học, bao gồm:
- Hệ thống phát chùm tia được đảm bảo chất lượng, có khả năng đạt suất liều tức thời rất cao (≥100 Gy/s).
- Các thiết bị đo liều theo thời gian thực vẫn duy trì tính tuyến tính trong điều kiện suất liều cực cao.
- Phần mềm lập kế hoạch điều trị có thể tích hợp các hiệu ứng sinh học phụ thuộc suất liều.
- Hiểu biết đầy đủ về cách các thông số vật lý và sinh học ảnh hưởng đến mức độ bảo vệ mô lành do hiệu ứng FLASH.
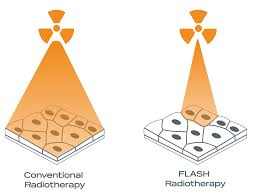
Cho đến nay, xạ trị UHDR sử dụng electron là hướng phát triển nhanh nhất. Các electron năng lượng 6–10 MeV có thể được tạo ra từ các máy gia tốc tuyến tính lâm sàng được cải tiến ở mức vừa phải, và đã có thể đạt suất liều UHDR đối với các tổn thương nông, mặc dù độ xuyên sâu thực tế chỉ khoảng 2–3 cm. Trong khi đó, FLASH sử dụng photon năng lượng megavolt vẫn là một thách thức kỹ thuật đang được nghiên cứu.
Liệu pháp proton đặc trưng bởi đỉnh Bragg (Bragg peak) và sự suy giảm liều rất nhanh sau điểm dừng, mang lại lợi thế so với electron hoặc photon trong việc giảm tổng liều tích lũy lên mô lành. Ion nặng còn bổ sung thêm một chiều kích sinh học bức xạ, vì chúng tạo ra các vệt ion hóa có chuyển năng lượng tuyến tính cao (High Linear Energy Transfer – LET), vốn ít bị ảnh hưởng bởi tình trạng thiếu oxy của khối u.
Việc kết hợp liệu pháp proton quét chùm bút chì (Pencil Beam Scanning – PBS) với suất liều FLASH có tiềm năng tăng cường bảo vệ mô lành trong khi vẫn duy trì độ phù hợp của phân bố liều. Các nghiên cứu tiền lâm sàng ban đầu sử dụng chùm proton truyền xuyên (transmission proton beams) ở suất liều UHDR đã cho thấy: giảm xơ hóa phổi, giảm độc tính da so với chiếu xạ proton ở suất liều thông thường, trong khi khả năng kiểm soát khối u vẫn được duy trì.
Tuy nhiên, proton UHDR cho đến nay chủ yếu sử dụng các chùm proton đơn năng lượng có dòng cao dạng “shoot-through”, nhằm bỏ qua thời gian chuyển đổi năng lượng chậm của cyclotron và synchrotron, đồng thời duy trì suất liều ≥40 Gy/s. Mặc dù điều này đã cho phép thực hiện các thử nghiệm đầu tiên trên người, nhưng nó đồng thời làm mất đi hai ưu điểm quan trọng của liệu pháp proton truyền thống: Liều thoát (exit dose) xuất hiện trở lại, vì chùm proton phải xuyên qua cơ thể bệnh nhân thay vì dừng tại đỉnh Bragg; Bộ chặn chùm tia công suất cao phía sau bệnh nhân trở thành nguồn phát neutron thứ cấp, tạo thêm một thành phần liều phụ.
Đối với các bác sĩ lâm sàng và nhà nghiên cứu trong lĩnh vực xạ trị, đồng vị phóng xạ theo nhiều khía cạnh chính là nền tảng của ngành này. Không có gì ngạc nhiên khi chúng vẫn là một trong những công cụ tốt nhất để đưa liều điều trị hủy diệt (ablative) một cách có mục tiêu tới các khối u não, phụ khoa, tuyến tiền liệt và tuyến giáp. Tuy nhiên, chúng cũng đặt ra những thách thức đặc thù đối với bác sĩ lâm sàng, nhà vật lý y học và các cơ sở y tế sử dụng chúng, dẫn tới xu hướng quốc tế nhằm hạn chế việc sử dụng khi có các phương án thay thế tốt hơn. Dù là sử dụng nhiệt (LITT), tia X năng lượng thấp được cung cấp trong phẫu thuật, chùm photon dẫn hướng bằng MRI có khả năng thích ứng, các chùm tia FLASH bảo vệ mô lành, hay các hạt mang điện có đỉnh Bragg, mục tiêu chung vẫn là lắng đọng liều phá hủy chính xác tại vị trí cần thiết mà không mang theo các rủi ro vốn có của việc sử dụng đồng vị phóng xạ.
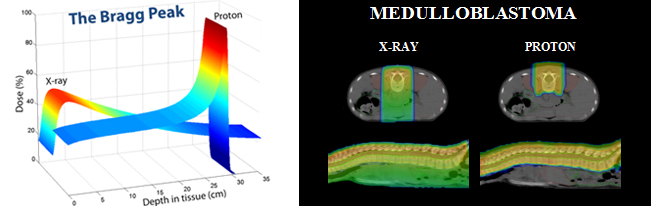
Nhìn chung, các phương thức này cung cấp một phổ rộng các lựa chọn điều trị lâm sàng:
- LITT cung cấp một phương án “từ trong ra ngoài” cho các tổn thương nằm sâu và khó tiếp cận bằng phẫu thuật.
- IORT và MR-LINAC giúp thu hẹp biên an toàn bằng cách sử dụng hình ảnh thời gian thực trong phòng mổ hoặc ngay trên bàn điều trị.
- FLASH khai thác yếu tố sinh học bức xạ liên quan đến suất liều để bảo vệ mô lành.
- Chùm proton hoặc ion nặng cho phép tập trung liều cao với liều thoát tối thiểu.
Tuy nhiên, không công nghệ nào trong số này hoàn hảo. Mỗi phương pháp đều yêu cầu thiết bị vốn đầu tư chuyên biệt, quy trình đảm bảo chất lượng nghiêm ngặt, và sự sẵn sàng áp dụng công nghệ mới thay cho các phương pháp đã được kiểm chứng lâu dài. Vì vậy, xạ trị áp sát dựa trên đồng vị phóng xạ vẫn không thể thay thế trong nhiều trường hợp, đặc biệt khi vi liều lượng đồng đều, khả năng tác động toàn thân, hoặc chi phí hạ tầng thấp là yếu tố quyết định trong điều trị. Do đó, xu hướng giảm phụ thuộc vào đồng vị phóng xạ có khả năng không phải là việc một công nghệ duy nhất thay thế hoàn toàn, mà sẽ là một tập hợp các phương thức điều trị, để bác sĩ lựa chọn giải pháp phù hợp nhất với hình học khối u, đặc điểm sinh học và điều kiện hậu cần của từng bệnh nhân.
Tiến bộ trong ba hướng chính sẽ quyết định tốc độ các công nghệ này trở thành thực hành lâm sàng thường quy:
- Thu nhỏ và tự động hóa thiết bị – chẳng hạn như hệ thống MRI di động, gantry proton nhỏ gọn, và các hệ thống FLASH tự che chắn, giúp mở rộng khả năng tiếp cận các công nghệ hiện chỉ có tại các trung tâm học thuật lớn.
- Sự hiệp đồng giữa các phương thức điều trị – ví dụ, sự phá vỡ hàng rào máu–não do LITT gây ra có thể tăng cường sự lắng đọng tại chỗ của các thuốc điều trị toàn thân, và tăng nhiệt dưới ngưỡng phá hủy có thể được kết hợp với liều IORT thấp hơn để đạt kiểm soát khối u.
- Hiểu biết cơ chế sâu hơn – chẳng hạn như làm rõ cơ sở phân tử của hiệu ứng FLASH, khả năng tăng nhạy bức xạ do nhiệt, và hóa học bức xạ của bức xạ LET cao. Những hiểu biết này sẽ giúp kê đơn các liệu pháp mới với mức độ tin cậy tương đương với các nguồn ¹⁹²Ir hoặc ¹²⁵I hiện nay.
Tóm lại, mặc dù lĩnh vực này đang chuyển dịch từ sự phân rã phóng xạ thụ động sang các phương thức phá hủy mô bằng năng lượng được tạo ra chủ động, lợi ích lâm sàng sẽ đến từ việc sử dụng đúng công cụ cho từng trường hợp, chứ không nhất thiết phải thay thế hoàn toàn một công nghệ bằng công nghệ khác.
Từ khóa: Xạ trị;
– CMD –






